Гидрид - германий
Cтраница 4
Из отфильтрованного гидрида был получен германий, в котором содержание примесей, указанных в таблице, снизилось по крайней мерена один - два порядка. Другим подтверждением наличия в гидриде германия взвешенных частиц может служить следующий эксперимент. Давно было замечено, что при длительном хранении германа в баллонах появляется налет светло-или темно-коричневого цвета. Для выяснения состава налета нами был изготовлен специальный разборный контейнер с ампулой из особо чистого кварцевого стекла. [46]
Моно - и дигерман - бесцветные газы, остальные - жидкости. Ниже приведены некоторые основные свойства гидридов германия. [47]
Способы получения гидридов германия во многом напоминают способы получения гидридов кремния. Основное отличие заключается в том, что гидриды германия легко получаются и в водных растворах. [48]
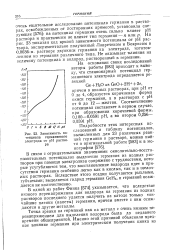 |
Зависимость потенциала германиевого электрода от рН раствора. [49] |
В связи с отрицательными значениями окислительно-восстановительных потенциалов выделение германия из водных растворов при помощи электролиза сопряжено с трудностями, которые усугубляются тем, что восстановление водорода идет в присутствии германия особенно легко как в кислых, так и в щелочных растворах. Вследствие этого осадки получаются рыхлыми, губчатыми; выделяется гидрид германия GeH, и германий осаждается не количественно. [50]
VIIA, формулы которых приведены в табл. 14.2, при обычных условиях находятся в газообразном состоянии. В молекулах метана СН4, гидрида кремния ( силана) SiH4, гидрида германия ( германа) GeH4 и гидрида олова ( станнана) SnH4 связывающие орбитали центральных атомов находятся в состоянии вр3 - гибридизации, а сами молекулы имеют тетраэдрическую форму. Однако из-за наличия несвязывающих электронных пар молекула NH3 имеет форму тригональной пирамиды, а молекула Н2О - угловую форму. [51]
Несколько особняком в химии Ge, Sn и Pb стоят их водородные соединения. Для двухвалентных элементов они не характерны, а для четырехвалентных устойчивость их в ряду Ge - Sn - Pb уменьшается настолько быстро, что существование РЬН4 могло быть доказано ( по летучести свинца при его соприкосновении с атомарным водородом), но в индивидуальном состоянии он не получар - Гидриды германия и олова образуются как незначитель-ные. От водорода они могут быть отделены охлаждением смеси газов жидким воздухом. [52]
Страницы: 1 2 3 4