Солеподобный гидрид
Cтраница 1
Солеподобные гидриды образуют активные металлы, а именно: ще лочные и щелочноземельные. [1]
Соединения водорода могут быть подразделены на три боль шие группы: солеподобные гидриды активных металлов ( LiH, СаН2 и др.), ковалентные водородные соединения р-элементов ( В2Н6, СН4, NH3, H2O, HF и др.) и металлоподобные фазы, образуемые d - и / - элементами; последние обычно являются нестехио-метрическими соединениями и часто трудно решить, относить ли их к индивидуальным соединениям или твердым растворам ( например, гидрид титана состава ПН еот а. Известны также соединения, занимающие промежуточное положение между указанными тремя группами. [2]
Водород со многими металлами образует твердые растворы и химические соединения, включая солеподобные гидриды. [3]
Соединения водорода с металлами и неметаллами могут быть подразделены на три большие группы: солеподобные гидриды активных металлов ( UH, CaHj и др.), ковалентиые водородные соединения р-элемеитов ( BjHe, СШ, МНэ, HjO, HF и др.) и металлоподобные фазы, образуемые d - и / - элементами; последние обычно являются нестехиометрическими соединениями, и часто трудно решить, относить ли их к индивидуальным соединениям или к твердым растворам ( например, гидрид титана состава TlHi607 2 oo) - Известны также соединения, занимающие промежуточное положение между указанными трема группами. [4]
Этот метод применим для получения металлов, не реагирующих с водой и не способных к образованию солеподобных гидридов. Поскольку восстановление происходит уже при сравнительно низких температурах, существует возможность получения металлов в высокодисперсном состоянии. Поэтому такой метод применяют премущественно для получения пирофоров, а также катализаторов. [5]
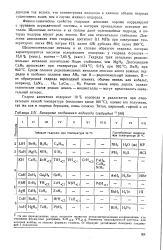 |
Бинарные соединения водорода ( гидриды. [6] |
Физико-химические свойства гидридов довольно хорошо коррелируют с группами периодической системы, к которым принадлежат исходные металлы. Щелочные металлы и их сплавы дают солеподобные гидриды, в которых водород играет роль аниона. [7]
Прочность связи водорода с металлами в этом случае характеризуется величиной теплоты образования соответствующего соединения. Так, щелочные и щелочноземельные металлы образуют солеподобные гидриды ( 1 - 2 ряд), а металлы 3 - 5 рядов - металлоподобные гидриды типа интерметаллических соединений. Металлы 6 - 10 рядов значительно меньше растворяют водород, чем металлы предыдущих рядов, но образуют прочные соединения как при низких, так и при высоких температурах, причем с повышением температуры поглощение водорода увеличивается. [8]
Среди бинарных соединений водорода различают следующие их группы: солеподобные гидриды s - элементов группы IA, щелочноземельных металлов, металлоподобные гидриды d - и / - элементов, ковалентные водородные соединения - элементов. [9]
Среди бинарных соединений водорода различают следующие их группы: солеподобные гидриды s - элементов группы IA, щелочноземельных металлов, металлоподобные гидриды d - и / - элементов, ковалентные водородные соединения р-элементов. [10]
Среди бинарных соединений водорода различают следующие их группы: солеподобные гидриды s - элементов группы IA, щелочноземельных металлов, металлоподобные гидриды d - и / - элементов, ковалентные водородные соединения / э-элементов. [11]
Среди бинарных соединений водорода различают следующие их группы: солеподобные гидриды s - элементов группы IA, щелочноземельных металлов, металлоподобные гидриды d - и / - элементов, ковалентные водородные соединения / э-элементов. [12]
Металлы побочных подгрупп, значительно отличающиеся иногда друг от друга своей химической природой, также образуют с водородом гидриды различного характера. Одни иЗ этих металлов ( например, лантан) образуют твердые солеподобные гидриды ( La3 H3 -), другие - твердые гидриды адсорбционного типа, выделяю - щие водород при нагревании; примером может служить палладий, 1 объем которого способен поглотить, вспучиваясь при этом, до 700 объемов водорода при обычных условиях. Третьи - твердые гидриды типа сплавов ( интерметаллические сплавы, сплавы-твердые растворы); поглощение водорода в таких случаях с нагреванием усиливается, как например у платины. [13]
Радиоактивный изотоп 24Ка ( Г, 2 15 ч) применяют в биологических и медицинских исследованиях. Природный карбонат натрия NaaCOs ( сода) был известен в древности и применялся как моющее средство. На воздухе окисляется, поэтому его хранят под слоем керосина. В зависимости от условий при взаимодействии с кислородом образуется оксид Na2O или пероксид NaaOa. Энергично взаимодействует с водой, кислотами, галогенами, серой, фосфором. С водородом при нагревании образует солеподобный гидрид NaH, с аммиаком - амид натрия NaNHs. Соли натрия окрашивают пламя в желтый цвет. [14]
Страницы: 1