Гидрирование - вещество
Cтраница 1
Гидрирование веех веществ проводилось в 96 % - ном перегнанном этаноле. [2]
Гидрированием вещества Д получают соединение Е состава 44 18 % ( масс.) С, 8 82 % Н и 47 % О. При взаимодействии 13 6 г вещества Е с 40 8 г уксусного ангидрида образуются вещество Ж и уксусная кислота. [3]
При гидрировании вещества поглотилось 6 1 мл водорода ( НТД); таким образом, смесь состоит из 0 069 г трифенилэтилена и 0 321 г три-фенилэтана. [4]
Реализуется он при гидрировании веществ, легко и полно снимающих водород с поверхности катализаторов ( хинон, нитробензол, винилацетилен и др.) - Энергия активации таких реакций характерна для процесса атомизации водорода; она практически одинакова при гидрировании любых соединений и достигает 12 - 14 ккал / моль. Скорость гидрирования таких соединений не зависит от рН раствора. Возможны промежуточные случаи, когда степень покрытия поверхности катализатора водородом является функцией строения гидрируемого соединения. [5]
Водородный эквивалент определяет расход водорода на гидрирование вещества в заданный момент реакции. [6]
Какой вывод следует из этого для реакции гидрирования ненатсшщенвых веществ, адсорбционный коэффициент которых больше, чем у водорода. [7]
Далее, рядом исследователей было замечено, что успешное гидрирование веществ, содержащих основный азот, облегчается в некоторых случаях использованием кислотных катализаторов. [8]
Была также проверена возможность действия этих окисляющих агентов на двойную связь подлежащего гидрированию вещества. [9]
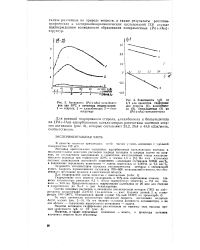
Пользуясь графиком ( см. рис. 46 и 47), определяют время, требующееся для гидрирования вещества наполовину ( оно характеризует активность катализатора), и количество водорода ( при 0 и 760 мм рт. ст.), поглощенного малеиновой кислотой, принимая в расчет количество водорода, поглощенного катализатором. Количество водорода, поглощаемого палладиевым катализатором, получают из графика, а количество водорода, поглощаемого окисью платины ( РЮ2 - Н2О), рассчитывают по весу окиси платины. [10]
Первым по ходу был помещен ГИАП-943-Н, который в течение примерно 3400 ч работал как поглотитель, а затем как катализатор деструкции и гидрирования сероорганических веществ до углеводородов и сероводорода. Данная система по поведению на ней СО, СО2, сероорганических веществ и H2S практически ничем не отличается от двухступенчатой схемы. Гидрирование СО не имеет места, а гидрирование СО2 идет на 22 - 36 %; наличие 1 0 - 1 5 % паров Н2О не мешает ни каталитическим процессам превращения сероорганических веществ, ни хемосорбции сероводорода. [11]
При некдторых процессах гидрирования в гидрируемое вещество вводят зеленый контакт, причем сначала я большей или менъгаой степени восстанавливается золений контакт и лишь после этого начинается гидрирование вещества. [12]
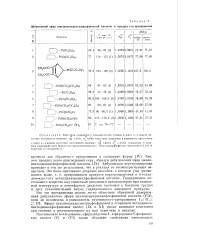 |
Дибутиловый эфир циклопентадиенилфссфикистой кислоты и продукт его превращения. [13] |
Арбузовская перегруппировка приводит к тем же результатам, что и реакция со свежеперегнанным веществом. Гидрирование постоявшего вещества над скелетным никелевым катализатором при комнатной температуре и атмосферном давлении протекает с большим трудом и дает незначительный выход гидрированного димерного продукта. [14]
Количество вводимого в реакцию водорода также имеет в ряде случаев существенное значение. В частности, при гидрировании фурановых веществ с платиновыми, палладиевыми и никелевыми катализаторами процесс, таким образом, может быть остановлен на стадии восстановления этиленовых связей в боковой цепи или продолжен до насыщения двойных связей цикла. [15]
Страницы: 1 2