Дифференцирование - величина
Cтраница 1
Дифференцирование величины М по К и () осуществлялось при неизменной Dz, что позволило принять величину L f ( Lnf D2), согласно (3.18) и (3.19), постоянной. [2]
При дифференцировании величины dalt dx2 рассматриваются как постоянные. [3]
Они возникли за счет дифференцирования величин, пропорциональных г3, г2 и г, и выражают соответствующие отношения числа измерений поверхностных, линейных и объемных элементов кристалла. [4]
Уравнение ( 3.1 Зв) получается дифференцированием величины J Z по в и приравниванием ее к нулю. В уравнении (4.3) AM соответствует произведению со и параметра потерь Ь, и его следует дифференцировать с учетом этого. Если потери малы, то трудностей и явных противоречий не возникает. [5]
На вход симметричного триггера поступают импульсы, получаемые путем дифференцирования величины v в схеме запоминания максимума. [6]
Угловая скорость и угловое ускорение вращения коромысла определяются, как и обычно, дифференцированием величины а, определяемой из равенства ( 15), по параметру времени. [7]
 |
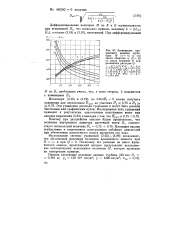
Схема измерения приращения выхода. а - принцип измерения. б - схемная реализация. [8] |
При поиске с измерением производной по времени показателем экстремума является соотношение скоростей изменения функции и аргумента. Схемы дифференцирования величин подробно рассматриваются в курсах счетно-решающей техники и поэтому здесь не описываются. [9]
Коэффициенты 2 / 3 и 7з часто встречаются в термодинамике дисперсных систем. Они появляются при дифференцировании величин, пропорциональных г3, г2 к г, к выражают отношение чисел измерений поверхностных, линейных и объемных элементов кристалла. [10]
Здесь первое уравнение системы характеризует изменение числа молекул газа в элементарном фазовом объеме [ г, r - f - dr ], [ v, vj dvj ] за промежуток времени dt, вызванное соударениями молекул между собой, а также соударениями молекул газа с твердыми частицами. Точка над любой величиной означает дифференцирование величины по времени вдоль траектории частицы. [11]
Сочетание значений AGS, AG / j с калориметрическими данными об энтальпиях растворения ( гидратации) позволяет вычислить энтропийные характеристики для тех же процессов переноса. Вычисление энтропии из температурной зависимости гиббсовых энергий, на наш взгляд, практического значения для водных растворов неэлектролитов не имеет. Во-первых, нет независимых данных о температурной зависимости Y-T, и, во-вторых, полученные путем дифференцирования величины заведомо менее точны. [12]
Страницы: 1