Гидрирование - двойная углерод-углеродная связь
Cтраница 1
Солективное гидрирование двойной углерод-углеродной связи с сохранением карбонильной группы легко осуществить для кетонов, функциональная группа которых менее реакционноспособна, чем в альдегидах. Катализаторами могут служить платина, никель, медь и другие металлические, но не оксидные контакты. Условия процесса существенно не отличаются от применяемых при гидрировании олефинов, но при выборе условий следует учитывать возможное побочное восстановление кетонной группы. В случае ненасыщенных альдегидов гидрирование только этиленовой связи предггавляет собой более сложную задачу. Для этого необходимы возмэжно более мягкие условия и катализаторы, мало активные в отношении гидрирования карбонильных групп. [1]
О гидрировании двойных углерод-углеродных связей в при - - сутствии карбонильных групп см. разд. [2]
Хаафу и Коху [2] удалось, как было описано выше, осуществить гидрирование двойной углерод-углеродной связи при действии на олефин парафиновых углеводородов в муравьиной кислоте с добавкой серной кислоты. [3]
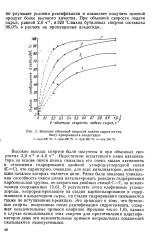 |
Влияние объемной скорости подачи сырья на глубину превращения альдегидов. [4] |
Недостатком испытанного нами катализатора на основе окиси цинка оказалась его очень малая активность в отношении гидрирования двойной углерод-углеродной связи ( СС), что характерно, очевидно, для всех катализаторов, действующим началом которых является цинк. В результате этого олефиновые углеводороды, непрореагировавшие на стадии карбонилирования и содержащиеся в альдегидном сырье, на стадии гидрирования оказываются также не вступившими в реакцию. Это приводит к тому, что бутиловые спирты, полученные после ректификации гидрогенизата, содержат незначительные примеси олефинов ( бромное число 1 0), однако в случае использования этих спиртов для приготовления пластификаторов даже эти незначительные примеси непредельных соединений оказываются недопустимыми. [5]
Для каталитического гидрирования карбонильных соединений и их аналогов можно использовать те же катализаторы, что и для гидрирования двойной углерод-углеродной связи ( см. разд. В лаборатории употребляют, в частности, скелетный никель, платину и палладий. [6]
Для каталитического гидрирования карбонильных соединений и их аналогов можно использовать те же катализаторы, что и для гидрирования двойной углерод-углеродной связи. [7]
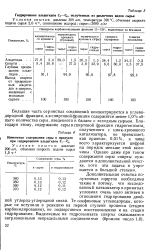 |
Гидрирование альдегидов С7 - Сд, полученных из различных видов сырья. [8] |
Дополнительная очистка полученных спиртов необходима также и потому, что исследованный катализатор в принятых условиях очень мало активен в отношении гидрирования двойной углерод-углеродной связи. Те олефиновые углеводороды, которые не вступили в реакцию на первой ступени процесса ( стадии карбонилирования), не подвергаются восстановлению и на стадии гидрирования. [9]
Интересно отметить, что при аналогичных условиях ацетон не гидрируется. В условиях опыта не происходит гидрирование двойной углерод-углеродной связи. [10]
Известно, что в присутствии никеля, кобальта, меди, платины, палладия и рутения восстановление СОО-группы протекает в более жестких условиях, чем гидрирование двойных углерод-углеродных связей. [11]
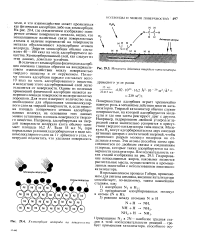 |
Хемисорбция водорода на поверхности.| Механизм действия твердого катализатора. [12] |
Поверхностная адсорбция играет чрезвычайно важную роль в механизме действия многих катализаторов. Твердый катализатор обычно служит поверхностью, на которой адсорбируются молекулы и где они затем реагируют друг с другом. Например, гидрирование двойной углерод-углеродной связи значительно ускоряется в присутствии твердого катализатора типа никеля. Молекулы Н2 могут адсорбироваться на двух соседних активных центрах с достаточной энергией, чтобы произошел разрыв молекул водорода на отдельные атомы. Эти атомы способны затем присоединяться по двойным связям к соединениям углерода, которые также адсорбируются на поверхности катализатора. Последовательность таких стадий изображена на рис. 29.5. Гидрирование ненасыщенных жиров, каковыми являются растительные масла, осуществляется в промышленных масштабах с использованием никелевого катализатора. [13]
По активности в процессах с участием водорода медные катализаторы уступают платиновым металлам, никелю, кобальту, однако по селективности превосходят их. Благодаря этим особенностям катализаторы на основе меди относительно редко применяются при гидрировании соединений с изолированной СС-связью. Значительно чаще их используют для гидрирования двойной углерод-углеродной связи, сопряженной с другими кратными связями ( СО, CN, ароматические кольца), которые при этом не затрагиваются. Например, при гидрировании ненасыщенных карбонильных соединений образуются насыщенные карбонильные соединения, в то время как на металлах VIII группы насыщаются все кратные связи, а на цинковых катализаторах образуются ненасыщенные спирты. [14]
Катализаторы реакций гидрирования - дегидрирования имеют разную активность, зависящую не только от состава, но и от способа приготовления и применения. При прочих равных условиях активность можно охарактеризовать температурой, при которой они способны катализировать определенный процесс, или скоростью реакции при постоянной температуре. Если взять в качестве эталона гидрирование двойной углерод-углеродной связи, то наиболее активными оказываются Rh, Pd, Pt и Ni, с которыми реакция идет уже при комнатной температуре. Эти металлы на носителях менее активны, и, например, с никелем высокая скорость достигается только при 100 - 150 С. Железо, медь и кобальт эффективны при 150 - 300 С, так же, как окись хрома и хромиты, а окислы и сульфиды молибдена и вольфрама - при 300 - 400 С. Приведенная характеристика активности контактов неуниверсальна и существенно меняется в зависимости от типа гидрируемой связи или функциональной группы. [15]
Страницы: 1 2