Кроветворная активность
Cтраница 1
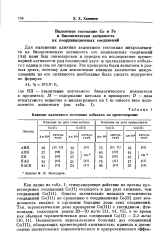
Зависимость кроветворной активности координационных соединений кобальта от константы устойчивости иллюстрируется данными табл. 7 и 8, из которых видно, что с ростом константы устойчивости соединений кобальта с жирными аминами и производными пиридина наблюдается тенденция к росту биологической активности. По данным Н. Б. Насельского [88], лизинат кобальта при содержании кобальта, вдвое меньшем, чем в аквокомплексе, в 2 раза быстрее восстанавливает как гемоглобин, так и содержание железа в крови. [1]
Большинство средств и методов защиты стимулирует кроветворную активность, что чаще всего и лежит в основе протективного действия. [2]
Таким образом, несмотря на некоторые исключения каталитическая и кроветворная активность в большинстве случаев увеличивается параллельно. [3]
В ряде случаев обнаружен параллелизм между каталитической активностью ( по разложению Н2Ог) и кроветворной активностью координационных соединений Sd-металлов. [4]
Выявлено, что комплексы меди с органическими лигандами в зависимости от хелатного узла могут подавлять или увеличивать кроветворную активность меди по сравнению с ее аквокомплексом. Так, хелатный узел аниона никелиновой кислоты и 8-аксихинолина подавляет ее, а алифатический азот, наоборот, увеличивает активность. При увеличении биологической активности микроэлемента хелатным узлом в ряде случаев с ростом константы устойчивости растет и биологическая активность координационного соединения. [5]
Интересно, что и каталитическая активность по разложению Н202, которая, как нами было показано, связана с кроветворной активностью для соединений Со ( П) и Gu ( II), также меняется с изменением константы устойчивости различно. Со ( ПК) 2 значительно быстрее разлагает Н202, чем нон [ Со ( Н20) 6 ] 2, в то время как при переходе от [ Си ( Н2О6) ] 2 к Си ( ПК) з медь почти полностью теряет свою каталитическую активность. [6]
 |
Влияние валентного состояния кобальта на кроветворение. [7] |
Для выяснения влияния валентного состояния микроэлемента на биологическую активность его комплексных соединений ( Ак) нами был синтезирован и передан на исследование кроветворной активности ряд соединений двух - и трехвалентного кобальта с одним и тем же лигандом. [8]
Конечно, нельзя сказать, что механизм защитного действия эстрогенов выяснен, но имеются веские доказательства в пользу того, что это действие связано с изменениями кроветворной активности, сопровождающими введение эстрогенов. Нет сомнения в том, что предварительное введение этих гормонов перед облучением может оказывать значительное защитное действие. [9]
Увеличение или подавление биологической активности при комплексообразовании зависит от природы донорных атомов ли-ганда, через которые осуществляется связь с медью, например координация к металлу первичных аминов резко увеличивает кроветворную активность меди. Активирующее же влияние пиридинового азота выражено несколько слабее, а при пятичленном циклообразовании с участием отрицательно заряженного кислорода активность меди подавляется. [10]
Доказательством того, что комплексное соединение оказывает действие при введении в организм без предварительного обмена лигандов, может служить следующий пример: при переходе от [ Со ( Н20) в ] 2 к Со ( ПК) 2 кроветворная активность растет, в то время как при переходе от [ Сн ( Н2О) е ] 2 к Си ( ПК) 2, наоборот, она значительно падает. Понятно, что если бы биологическую активность проявлял ион [ М ( Н20) в ] 2, то для обоих металлов с увеличением константы устойчивости соединения активность должна была бы изменяться в одном направлении, чего на практике не наблюдается. [11]
Образцы были переданы в Институт фармакологии и химиотерапии АМН СССР, на кафедру фармакологии, в Отдел фармакологии проблемной лаборатории Ташкентского фармацевтического института для изучения именно этих свойств. Поэтому, когда речь идет о биологической активности препаратов, следует понимать ее в смысле кроветворной активности, так как вещества, не обладающие ею, могут проявлять активность в других биологических процессах, протекающих в организме. [12]
При разложении комплекса в организме образовавшиеся свободные ионы меди, независимо от того, с каким атомом ( хелатным узлом) они предварительно были связаны, должны были бы проявлять одинаковое действие. Однако экспериментальные данные свидетельствуют о другом. Так, три соединения меди: с пиколи-новой кислотой, ятреном и триэтилентетрамином, имеющие близкие по значению величины констант устойчивости, обладают резко различной кроветворной активностью; первые два почти совершенно неактивны, а третье проявляет значительную активность. [13]
Положительная или отрицательная биологическая активность рассмотренных в таблице соединений является следствием фармакологического действия самих лигандов. Ахмадие-вой [97] установлено, что никотинамид ( витамин РР) обладает гемопоэтическими свойствами. Изоникотиновая же кислота так же, как и ее амид и этиловый эфир, витаминными свойствами не обладает и поэтому не обладает, возможно, и кроветворной активностью. [14]
Страницы: 1