Гидроксид - алюминий
Cтраница 1
Гидроксид алюминия, согласно указанным уравнениям реакций, ведет себя в отношэнии щелочей как кислота. [1]
Гидроксид алюминия А1 ( ОН) 3 имеет амсротерный характер. [2]
Гидроксид алюминия при нагревании довольно трудно теряет воду. Следы воды удаляются при очень сильном прокаливании. Наоборот, оксид алюминия способен поглощать воду из воздуха, которая постепенно может из адсорбированной переходить в химически связанную. Это свойство оксида алюминия сохраняется в катализаторе. Приготовленные на основе гидроксида алюминия катализаторы обладают некоторой гигроскопичностью, в результате чего они могут увлажняться и терять свою активность. Так, алю-момолибденовый катализатор после прокаливания при 650 С, находясь на воздухе, довольно быстро поглощает влагу. Поэтому влажность катализаторов, осажденных на гидроксиде алюминия, определяют при тех же температурах, при которых удаляется остаток воды. Как предусмотрено техническими условиями, содержание воды в алюмосиликатном катализаторе определяют при 800 С, а алюмомолибденового - при 650 С. При этом вместе с удалением воды происходит некоторое разложение катализатора с удалением в основном его органических примесей. [3]
Гидроксид алюминия используют в производстве солей алюминия. [4]
Гидроксид алюминия получают в производственных масштабах переработкой глиноземсодержащего сырья, в основном бокситов нефелинов, а также каолинов, глин, золы и других алюмо -: иликатов. [5]
Гидроксид алюминия А1 ( ОН) з растворяется в избытке щелочи, образуя гидроксосоединение с координационным числом шесть. [6]
 |
Суруктура А1 ( ОН3. [7] |
Гидроксид алюминия А1 ( ОН) 3 может быть в двух видоизменениях: в кристаллической форме - бесцветные кристаллы моноклинической системы ( рис. 123), плотность 2 42, или в аморфной - белый студенистый осадок, получаемый при осаждении гидроксида из растворов солей алюминия едкими щелочами. ОН) 3 может быть получен и в виде метагидроокиси АЮОН белого цвета. [8]
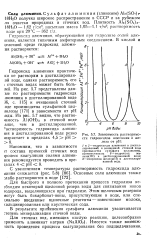 |
Зависимость растворимости гидроксидов алюминия и железа от рН. [9] |
Гидроксид алюминия, образующийся при гидролизе солей алю - 1иния, является типичным амф отерным соединением. [10]
Гидроксид алюминия нерастворим в средах с нейтральным рН, поэтому ион А13 не входит в число естественных примесей природных вод, однако может содержаться в них из-за попадания в речную воду промышленных отходов. В анализируемый водный раствор предварительно добавляют избыток фторид-ионов, которые образуют с А13 комплексный анион A1FJT, после чего раствор встряхивают со слабокислотной карбоксильной смолой. За исключением А1 ( Ш) все остальные ионы металлов поглощаются смолой. [11]
Гидроксид алюминия А1 ( ОН) з выпадает в виде студенистого осадка при действии щелочей на водные растворы солей алюминия. [12]
Гидроксиды алюминия и галлия амфотерны, но их кислотные свойства выражены значительно сильнее, чем основные. [13]
Гидроксид алюминия относится к слабым электролитам. [14]
Гидроксид алюминия, как и оксид, обладает амфо-терными свойствами. [15]
Страницы: 1 2 3 4