Гидроксид - четвертичный аммоний
Cтраница 1
Гидроксиды четвертичного аммония - чрезвычайно сильные основания, подобно гидроксидам натрия и калия. [1]
Действующим основанием в органическом растворителе служит гидроксид четвертичного аммония, который не способен координироваться с альдегидом и тем самым обеспечивать гидридный перенос. [2]
Соли четвертичного аммония при обработке их оксидом серебра образуют гидроксид четвертичного аммония ( 7.4 N OH -), являющийся сильной щелочью. [3]
Соли четвертичного аммония при обработке их оксидом серебра образуют гидроксид четвертичного аммония ( i.4 N OH -), являющийся сильной щелочью. [4]
Применение гидроксида тетрабутиламмония в качестве тит-ранта сильно расширило применимость титриметрических методов для определения енолов и фенолов, исследованных Фрицем [12], который использовал раствор метилата натрия в смеси бензола и метанола, а в качестве среды - диметилформамид или этиленди-амин Метод Фрица является модификацией метода Мосса, Эллиота и Холла [13], которые применяли этилендиамин в качестве растворителя и натриевую соль этаноламина в качестве титранта. Гидроксид четвертичного аммония является очень сильным основание. [5]
Применение гидроксида тетрабутиламмония в качестве тит-ранта сильно расширило применимость титриметрических методов для определения енолов и фенолов, исследованных Фрицем [12], который использовал раствор метилата натрия в смеси бензола и метанола, а в качестве среды - диметилформамид или этиленди-амин Метод Фрица является модификацией метода Мосса, Эллиота и Холла [13], которые применяли этилендиамин в качестве растворителя и натриевую соль этаноламина в качестве титранта. Гидроксид четвертичного аммония является очень сильным основанием, растворимым в органических растворителях. [6]
Из этого следует, что при нормальном механизме МФК не следует ожидать простой линейной зависимости от концентрации катализатора. Изменения в скорости реакции, полученные при варьировании концентрации гидроксида натрия в водной фазе и добавления в-нее бромида, также не согласовывались с предположением о том, что эти изменения связаны с простой экстракцией гидроксида четвертичного аммония в органическую фазу. Хотя общее уравнение кинетики реакции вывести не удалось, полученные данные лучше всего соответствуют механизму, рассмотренному выше. [7]
Ионообменные смолы позволяют производить полную замену одного иона на другой. Например, если раствор натриевой соли карбоновой кислоты пропускать через колонку сильнокислотного катионита, находящегося в форме свободной кислоты ( Н - форма), то все ионы натрия в растворе заменяются на протоны, и из колонки элюируется только карбоновая кислота. Этот способ удобен для выделения некоторых растворимых в воде кислот из растворов их солей; его можно рассматривать как один из примеров использования реагентов на полимерных носителях. Элюат будет содержать только гидроксид четвертичного аммония; этот способ весьма удобен для получения таких соединений. [8]
Наиболее простой механизм МФК в присутствии сильных щелочей ( например, механизмы H / D-обмена и изомеризации), по всей видимости, включают экстракцию гидроксида. Многие другие механизмы глубоко не изучены. В случае МФК механизмы могут сильно изменяться в зависимости от характера субстрата и условий реакции. Так, например, - элиминирование может проходить межфазно, если катализатор облегчает стадию депротонирования. В то же время, если в органической фазе присутствуют малые количества ионов гидроксида четвертичного аммония, то и депротонирование будет осуществляться в этой же фазе. Однако известен еще и третий механизм. Он наблюдается в отсутствие оснований при повышенных температурах. В неполярных средах относительно несольватированные ионы галогенидов ведут себя как основания ( см. гл. [9]
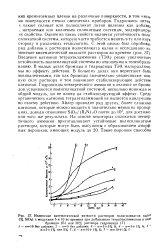 |
Изменение кинематической вязкости растворов полисиликатов кали ( % SiCb с модулями 5 и 10 во времени при добавлении тетраэтиламмония в виДе. [10] |
Гидроокись лития 1 также силикат или полисиликат лития полезны как добав, натриевым или калиевым силикатным системам, модифицируя свойства. Одним из таких свойств является устойчивость поли-силикатной системы, которую часто требуется менять в ту или иную сторону в различных технологиях. Введение катионов тетраэтиламмония ( ТЭА) резко увеличивает устойчивость полисиликатной системы по отношению к гелеобразо-ванию. В малых дозах бромиды и гидроксиды ТЭА малоразличимы по эффекту действия. В больших дозах они перестают быть эквивалентными, так как бромиды значительно увеличивают ионную силу раствора и тем понижают стабилизирующее действие катионов. Гидроксиды четвертичного аммония в отличие от бромидов усваиваются полисиликатной системой, несколько понижая ее общий модуль, но не влияя на стабилизирующий эффект. Среди органических катионов тетраэтиламмоний не является наилучшим по своему действию. Дилер приводит ряд других, более сложных катионов, которые можно вводить в значительно меньших пропорциях, доводя отношение SiCb / ( R4N) 2О почти до 103, для достижения того же результата. [11]
Страницы: 1