Гидроксид - металл
Cтраница 1
Гидроксиды металлов, растворимые в воде. [1]
Гидроксиды металлов принято делить на две группы: растворимые в воде ( образованные щелочными и щелочноземельными металлами) и нерастворимые в воде. Основное различие между ними заключается в том, что концентрация ионов ОН - в растворах щелочей достаточно высока, для нерастворимых же оснований она определяется растворимостью вещества и обычно очень мала. Тем не менее, небольшие равновесные концентрации иона ОН даже в растворах нерастворимых оснований определяют свойства этого класса соединений. [2]
Гидроксиды металлов реагируют с образованием фторида металла и кислорода. [3]
Гидроксиды металлов - это соединения, в молекулах которых атомы металлов связаны с гидроксо-группами. Состав гидроксидов определяется окислительным числом металлического элемента и выражается формулой Me ( ОН) П, где п - окислительное число. Кроме таких однородных гидроксидов, часто встречаются смешанные оксид-гидроксиды состава Me ( ОН) 2тОт, где п-окислительное число металлического элемента, am - небольшие целые числа. Гидроксиды наиболее активных металлов характеризуются свойствами оснований. По мере уменьшения активности металлов свойства их гидроксидов изменяются от типично основных через амфотерные к кислотным. [4]
Гидроксиды металлов окисляются на влажном воздухе и образуется пероксид водорода. [5]
Гидроксиды металлов преимущественно образуют положительно заряженные коллоиды, а ядра из веществ кислотного характера образуют отрицательно заряженные коллоиды. На положительно заряженные коллоиды оказывает влияние анион, на отрицательно заряженные - катион. [6]
Гидроксиды металлов занимают промежуточное положение между этими двумя классами. [7]
Гидроксиды металлов осаждаются обычно не в чистом виде, а в соединении с некоторой долей неразложившейся соли - в форме основной соли. Примером может служить осаждение из хлоридных или сульфатных растворов гидроксида магния, который выделяется в виде основных солей непостоянного состава. Особенно прочные основные соли образуются при осаждении из сульфатных растворов. Избыток щелочи разлагает основные соли, но не всегда в полной мере. Вследствие больших пересыщении при осаждении и очень быстрого ( мгновенного) образования твердой фазы, она часто выделяется вначале в нестабильной форме, неравновесной с раствором. При дальнейшем контакте составы осадка и раствора постепенно изменяются и приходят в равновесие. Этот процесс иногда называют старением осадка. [8]
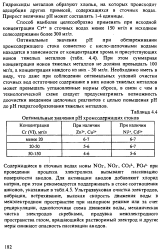 |
Оптимальные значения рН хромсодержащих стоков. [9] |
Гидроксиды металлов образуют хлопья, на которых происходит адсорбция других примесей, содержащихся в сточных водах. Прирост величины рН может составлять 1 - 4 единицы. [10]
 |
Свойства металлов IB-группы. [11] |
Гидроксиды металлов IB-группы получают действием на их соли растворов щелочей. Галиды серебра ( за исключением AgF) малорастворимы в воде и используются в качестве светочувствительных материалов. [12]
 |
Растворимость гидроксидов шелочных металлов. [13] |
Гидроксиды металлов IA-подгруппы представляют собой бесцветные кристаллические вещества. Их сила возрастает от LiOH к CsOH с увеличением радиуса катиона. За исключением LiOH, гидроксиды щелочных металлов термически устойчивы до температур выше 1000 С. [14]
Гидроксиды металлов IB-подгруппы получают действием на их соли растворов щелочей. Галогениды серебра ( за исключением AgF) мало растворимы в воде и используются в качестве светочувствительных материалов. [15]
Страницы: 1 2 3 4