Гидроксид - щелочноземельный металл
Cтраница 1
Гидроксиды щелочноземельных металлов обладают только основными свойствами. [1]
Гидроксиды щелочноземельных металлов, прежде всего, кальция и бария, трудно растворимы в воде, но полученные при этом разбавленные растворы тоже проявляют все свойства щелочей. [2]
Применение гидроксидов щелочноземельных металлов позволяет избежать замещения атома водорода. [3]
При взаимодействии с кислотами оксиды и гидроксиды щелочноземельных металлов легко образуют соответствующие соли, как правило, бесцветные. Из производных обычных минеральных кислот соли с анионами СГ, Вг -, Г и МОз хорошо растворимы; напротив, с анионами F, ЗОГ, СОз и POj малорастворимы в воде. В противоположность ионам Са и Sr ион Ва ядовит. Многие соли рассматриваемых элементов находят разнообразное практическое использование. [4]
Едкие щелочи NaOH, КОН и гидроксиды щелочноземельных металлов Са ( ОН) 2, Ва ( ОН) 2 при нагревании с солями аммония выделяют аммиак. [5]
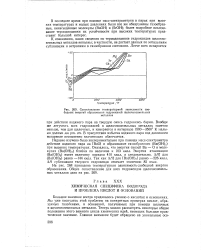 |
Сопоставление температурной зависимости свободных энергий образования гидроокисей щелочноземельных. [6] |
К сожалению, наши сведения по термодинамике гидроксидов щелочноземельных металлов неполны; в частности, не достает данных по энтальпиям сублимации и энтропиям в газообразном состоянии. [7]
При нагревании MoOj без доступа воздуха с гидроксидами щелочноземельных металлов образуются молибдаты ( 1У) M JMoOj и М 2М () О. [8]
Металлсодержащие присадки получают путем нейтрализации фосфоросернениых полимеров оксидами или гидроксидами щелочноземельных металлов. [9]
Обычно отделение железа, хрома, алюминия и титана от марганца ( II) и гидроксидов щелочноземельных металлов проводят при помощи буферного раствора, содержащего аммиак и хлорид аммония. Медь, цинк, никель и кобальт остаются в растворе в виде устойчивых аммиачных комплексов. В этих условиях часто образуются студенистые осадки, дальнейшая работа с которыми затруднительна. [10]
Таким образом, проведенные исследования показывают, что на процессы структурообразования большое влияние оказывают гидроксильные группы гидроксидов щелочноземельных металлов. В присутствии растворов NaOH и КОН структурные связи не только не формируются, но и разрушаются уже имеющиеся. [11]
 |
Схема строения линейного полимера. [12] |
Гидроксид бериллия Be ( ОН) 2 имеет ясно выраженный амфо-терный характер, чем резко отличается от гидроксидов щелочноземельных металлов. [13]
 |
Схема строения линейного полимера черные кружки - атомы бериллия. белые - атомы хлора. [14] |
Тидроксид бериллия Ве ( ОН) 2 имеет ясно выраженный амфо-терный характер, чем резко отличается от гидроксидов щелочноземельных металлов. [15]
Страницы: 1 2 3