Гидроксил-ионы
Cтраница 2
 |
Влияние температуры на Кш. [16] |
При диссоциации воды также образуются гидроксил-ионы и в равных количествах ионы водорода. [17]
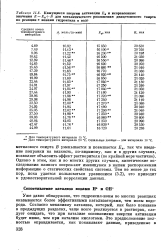 |
Кажущиеся энергии активации Еа и исправленные. [18] |
Уже давно обнаружено, что гидроксил-ионы во многих реакциях оказываются более эффективными катализаторами, чем ионы водорода. Согласно механизму катализа, который, как было показано в предыдущих разделах, чаще всего реализуется в растворах, следует ожидать, что при катализе основаниями энергия активации будет ниже, чем при катализе кислотами. [19]
Судьба этих ионов различна: гидроксил-ионы не вступают ни в какие реакции, остаются свободными и концентрация их поэтому возрастает; ионы водорода тотчас расходуются на образование уксусной кислоты, и, следовательно, их концентрация будет меньше концентрации гидроксил-ионов. Те ионы водорода, которые возникают и тотчас исчезают, играют роль как бы промежуточного продукта и не войдут в итоговое уравнение. [20]
 |
Ионные произведения некоторых растворителей при 25 С. [21] |
При диссоциации воды также образуются гидроксил-ионы и ионы водорода в равных количествах. [22]
Тогда можно считать, что гидроксил-ионы ОН - возникают при реакции алкоголята, вода достаточно слабо диссоциирует и ионами. [23]
Гибридизация орбиталей 74 Гидратация 24, 55 Гидроксил-ионы, концентрация 46 Гидроксильная группа 79 Гидроксоний-ионы 40 Гидролиз 51 ел. [24]
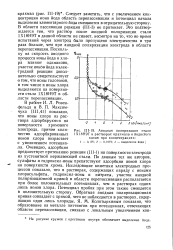 |
Анодная поляризация стали 1Х18Н9Т в растворах крахмала и йодистого. [25] |
По данным тех же авторов, сульфаты и гидроксил-ионы препятствуют адсорбции ионов хлора на поверхности хрома. Исследование кинетики электродных процессов показало, что в растворах, содержащих наряду с ионами хлорасульфаты, гидроксил-ионы и нитраты, участок анодной поляризационной кривой в области перепассивации располагается при более положительных потенциалах, чем в растворах одних лишь ионов хлора. Потенциал пробоя при этом также смещается в положительную сторону. Обратная анодная поляризационная кривая совпадает с прямой, чего не наблюдается в растворах, содержащих одни лишь хлориды. [26]
При обработке анионообменных смол солями по аналогичному механизму высвобождаются гидроксил-ионы. [27]
Щелочи в водных растворах распадаются ( диссоциируют) на гидроксил-ионы ОН и ионы металла или сложного радикала. [28]
Следовательно, в растворе амфотерного соединения содержатся ионы металла, гидроксил-ионы, ионы водорода и кислотного остатка. [29]
Для нейтрализации Минеральных кислот применяют любой щелочной реагент, дающий в растворе гидроксил-ионы ОН -; чаще всего применяют едкие, углекислые и двууглекислые щелочи. Гидроксид натрия и соду применяют только в тех случаях, когда эти реагенты являются отходами местного производства. [30]
Страницы: 1 2 3 4