Замещенный гидроксиламин
Cтраница 1
Замещенные гидроксиламины образуют N-замещенные оксн-сульфаминовые кислоты ( см. стр. [1]
Нитрозосоединение тем же путем превращается в замещенный гидроксиламин ( напишите схему превращений. Вследствие своей более высокой карбонильной активности нитрозосоединения гидрируются быстрее, чем нитросоединения, поэтому, как правило Нитрозосоединение не удается уловить во время восстановления. [2]
Реакция соответствует образованию нитронов из альдегидов и замещенных гидроксиламинов. [3]
В общем случае реакция с радикалами приводит к полностью замещенным гидроксиламинам; например, из нитро-зрметана и метильного радикала образуется триметилгидроксил-амин. Особенно хорошей ловушкой для гидроксильных радикалов служит n - нитрозодиметиланилин. Нитрозосоединения используют и как ингибиторы полимеризации. [4]
Пиролитическое разложение JV-окисей аминов, приводящее к образованию олефина и замещенного гидроксиламина ( реакция Коупа), является реакцией сын-элиминирования р-водорода под действием основания, так как здесь имеет место атака атома кислорода, связанного с азотом семиполярной связью. Af-Окись Ч с-диметил ( 2-фенилциклогексил) амина дает при разложении 3-фенилциклогексен. Термическое разложение Af-окиси диметил ( 1-ме-тилциклогексил) амина дает до 97 % метиленциклогексана, в то время как разложение сложных эфиров - только 25 % этого соединения. Сравнение термического разложения эфиров и N-окн-сей аминов показывает, что разложение Л - окисей более стерео-специфично. Препаративное значение имеет термическое разложение Af-окисей аминов, содержащих средние циклы. Окись циклооктилдиметиламина при термическом разложении дает только ыыс-циклооктен, аналогичная реакция девяти - и десяти-членных циклов приводит к гранс-циклоолефинам. [5]
Другим примером является перегруппировка Мейзенгеймера, в которой оксид третичного амина просто при нагревании перегруппировывается в замещенный гидроксиламин. [6]
Гамбарян [88,89] показал, что взаимодействие перекиси бензоила с алифатическими и ароматическими вторичными аминами приводит к образованию 0-бензоильного производного соответствующего замещенного гидроксиламина. [7]
Гамбарян [87, 88] показал, что взаимодействие перекиси бензоила с алифатическими и ароматическими вторичными аминами приводит к образованию О-бензоильного производного соответствующего замещенного гидроксиламина. [8]
Другой реакцией с аналогичным механизмом [300] является перегруппировка Мейзенгеймера [301], в которой оксид третичного амина перегруппировывается при нагревании в замещенный гидроксиламин. [9]
 |
Классическая ( 1 и переменно-токовые 2 3 полярограммыкетон-радикала ( 1 3 и триацетонамина ( 5 на фоне буферного раствора, рН 2 5 ( концентрация 1 - 10 - 3 М. [10] |
Методом циклической вольтамперометрии на ртутном и платиновом электродах и электролизом при контролируемом потенциале установлено [17], что продуктами электровосстановления являются соответствующие замещенные гидроксиламины. [11]
Гамбарян [87, 88] показал, что взаимодействие перекиси бензоила с алифатическими и ароматическими вторичными аминами приводит к образованию О-бензоильного производного соответствующего1 замещенного гидроксиламина. [12]
Пространственные затруднения, отчасти обусловливающие высокую стабильность иминоксилов, в меньшей мере отражаются на реакционной способности гидроксиламинов. С хлорангидридами карбоновых кислот, арилсульфохлоридами и фенилизоцианатом замещенные гидроксиламины образуют хорошо кристаллизующиеся производные, которые были использованы для установления структуры и идентификации продуктов восстановления иминок-сильных радикалов. [13]
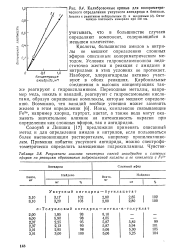 |
Результаты анализа некоторых, смесей ангидридов и сложных, эфиров по реакциям образования гидроксамовой кислоты и ее комплекса с. [14] |
Солоуэй и Липшиц [17] предложили применять описанный метод и для определения амидов и нитрилов, если пользоваться более высококипящим растворителем, например пропиленглико-лем. Применяя избыток уксусного ангидрида, можно спектрофо-тометрически определить замещенные гидроксиламины. [15]
Страницы: 1 2