Гидроксилирование - ароматическое кольцо
Cтраница 1
Гидроксилирование ароматического кольца в молекулах многих ядов является предпосылкой для дальнейшего его расщепления и проходит при участии донора водорода. [1]
Для гидроксилирования ароматических колец используется реактив Фентона, представляющий собой смесь пероксида водорода и сульфата железа ( II) [153, 154]; однако из-за побочного образования диарилов выходы основного продукта обычно низкие. [2]
В организме животных при метаболизме гербицидных мочевин кроме реакций N-деметилирования и N-деметоксилирования происходит еще и гидроксилирование ароматического кольца, причем все гидрокси-лированные метаболиты выводятся из организма в виде хорошо растворимых в воде глюкуронидов или сульфатов. [3]
Реакции этого типа весьма разнообразны: они лежат в основе превращения алканов в спирты, олефинов - в эпоксиды, сульфидов - в сульфоксиды; это реакции гидроксилирования ароматического кольца и его раскрытия, а также окислительного деметилирования. Вполне возможно, что результаты глубокого изучения механизма активации и: присоединение кислорода ферментами найдут применение для. В последнее время большое внимание уделялось использованию различных микробных оксигеназных систем в стереоспецифическом эпокси-окислении олефинов, в результате которого образуются строительные блоки для синтеза полимеров. В микроорганизмах-окисляющих алканы и алкены, функционируют соответствующие монооксигеназы, но если исходить из нынешнего уровня; технологии, то вряд ли хоть один процесс такого типа целесообразен с экономической точки зрения. Поскольку оксигеназы нестабильны, принято считать, что эти процессы основаны на биокаталитической активности целостных организмов. На первом этапе пиранозо-2 - оксидаза из гриба-ба-зидиомицета катализирует образование перекиси водорода, используя в качестве субстрата и источника энергии глюкозу. Далее галопероксидаза осуществляет реакцию перекиси водорода с алкеном и ионом какого-либо галогена с образованием алкенгалогидрина, от которого затем отщепляются атомы водорода и галогена и образуется соответствующий алкеноксид. Побочными продуктами процесса являются фруктоза и глюко-новая кислота. Стереоспецифичность окислительного катализа может использоваться в процессе синтеза диэпоксимономеро & для производства стереорегулярных полимеров. Мономерные, единицы могут быть получены и путем превращений бензола под действием оксигеназ гл, 5) или в результате двойного моноокисления дифенила с образованием 4 4-дигидроксидифенила. [4]
Механизм метаболизма пестицидов в почве под влиянием микроорганизмов сводится к следующим основным реакциям: дегалоиди-рование, дезалкилирование, амидный или эфирный гидролиз, окисление, восстановление, разрыв эфирной связи, гидроксилирование ароматического кольца и разрыв кольца. [5]
Среди них особо выделяются: 1) реакции присоединения, например образование гиппуровой кислоты из бензойной кислоты, образование сульфатов эфиров и ( 3-глюко-зидов, ацетилирование и метилирование; 2) реакции окисления, например алифатическое окисление, ароматическое окисление, эпоксидация, гидроксилирование ароматических колец и окисления тиофосфатных и пирофос-форамидных инсектицидов; 3) восстановление; 4) де-гидрохлорирование инсектицидов и, наконец, 5) детокси-кация ядов, содержащих тяжелые металлы, взаимодействием с соединениями серы. Ниже будет рассмотрен главным образом метаболизм хлор - и фосфорорганиче-ских инсектицидов. [6]
Гидроксилирование ароматического кольца происходит лишь в очень незначительной степени, приводя к образованию р-тетралола. [7]
Гидроксилирование ароматического кольца приводит к образованию 1 2 3 4-тетрагидронафталин - 6-ола. [8]
В сточных водах каучукового производства происходит биодеградация И. Основной путь окисления начинается с гидроксилирования ароматического кольца с дальнейшим образованием алифатической кетокислоты. [9]
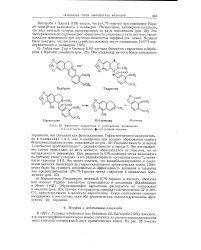 |
Биосинтез гидрастина и родственных алкалоидов. из - углерода тирозина. ф из 3-углерода тирозина. [10] |
Это показывает, что синтез происходит из двух молекул, образующихся из тирозина, но не находящихся в равновесии. Это может означать, что декарбоксилирование и соединение молекул происходят до гидроксилирования ароматических колец. Интересно было бы сравнить относительную эффективность допамина и тирамина как предшественников. [11]
Разложение аналогов ДДТ, содержащих в ароматическом ядре вместо атомов хлора алкильные, алкоксильные и сульфидные группы, протекает несколько иначе. Наряду с направлениями, характерными для метаболизма ДДТ, происходят и другие превращения: сульфидная сера окисляется до сульфонов и далее расщепляется с образованием сульфо-кислот; алкильные радикалы относительно быстро окисляются до кар-боновых кислот; наблюдается гидроксилирование ароматического кольца. Во всех случаях образуются гидрофильные соединения, которые легко выводятся из организма животных и не накапливаются в объектах окружающей среды. [12]
Страницы: 1