Ароматическое гидроксилирование
Cтраница 1
Ароматическое гидроксилирование in vitro осуществляется: ак реакция электрофильного замещения при взаимодействии фенов с пероксидом водорода в присутствии электрофильных катализаторов - хлорида алюминия или фтороводорода. [1]
Ароматическое гидроксилирование метаболитов диазепама характерно для организма крыс, а гидролитическое расщепление бенздиазепинового кольца с последующим ароматическим гидро-ксилированием - для организма кроликов. [2]
При ароматическом гидроксилировании гидрок-сильные радикалы получают главным образом из реактива Фентона или путем радиолиза воды ( гл. [3]
Аналогичные результаты получены при анодном ароматическом гидроксилировании. [4]
Метаболиты празепама в дальнейшем подвергаются ароматическому гидроксилированию с последующей глюкуроновой и сульфатной конъюгацией. [5]
Важной стадией биосинтеза многих природных соединений является ароматическое гидроксилирование. Такие реакции катализируются оксигеназами со смешанными функциями и обычно проходят с промежуточным образованием систем оксепин - аренок-сид. Имеется детальный обзор [52], посвященный этим гидридным перемещениям, которые будут рассмотрены в гл. [6]
Избыточное пероральное введение бромзепа-ма животным приводит к значительному гидролизу исходного вещества и последующему ароматическому гидроксилированию. Через сутки у крыс, собак, морских свинок и кроликов соединение LX XIV выводится в количестве 35 1; 51 7; 31 5 и 56 6 % введенной дозы бромазепама ( 50 мг / кг) соответственно. [7]
Для мышей основными метаболитами являются 3-окси-производное ( CIII), а также соединения CVI и CVII, для крыо - продукты ароматического гидроксилирования. [8]
Все соединения этого ряда, имеющие S-конфигурацию, обладаю; высокой фармакологической активностью, в то время как соединения с - конфигурацией ее лишены. Ароматическое гидроксилирование соединений, катализируемое ферментами, сте-реоспецифично, в то время как С3 - гидроксилирование и N-дезме-тилирование не обнаруживают такой специфичности. [9]
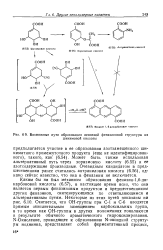 |
Возможные пути образования основной феназиновой структуры из. [10] |
Каким бы ни был механизм образования феназин-1 6-ди-карбоновой кислоты (6.57), в настоящее время ясно, что она является первым феназиновым продуктом и предшественником других феназинов, синтезирующихся по ответвляющимся и альтернативным путям. Некоторые из этих путей показаны на рис. 6.10. Считается, что ОН-группы при С-1 и С-6 вводятся прямым окислительным замещением карбоксильных групп, в то время как ОН-группы в других положениях появляются в результате обычного ароматического гидроксилирования. [11]
Оксираны находят широкое применение в синтетической органической химии, так как их циклическая система может легко создаваться и разрушаться с высокой степенью селективности. Лейкотриен А ( 2) представляет собой биосинтетический предшественник медленно действующего вещества и лейкотрие-нов, которые применяются при бронхиальной астме. Диспарлур ( 3) - феромон насекомого, половой аттрактант непарного шелкопряда, также содержит оксирановый фрагмент. Оксираны, получаемые из ароматических углеводородов ( арилоксиды), выступают в качестве промежуточных соединений в реакциях ароматического гидроксилирования в живых организмах. Этиленоксид и другие оксираны, получаемые из низших алкенов каталитической реакцией с кислородом, производятся в огромных количествах и используются в производстве полимеров. [12]
В работе Савады и соавторов [197] выяснены пути образования и механизм окисления у различных видов животных метаболита LXXIV. В опытах in vitro они установили, что предшественником соединения LXXIV в общем обмене бромазепама является вещество LXXIII. Наибольшей гидроксилирующей активностью обладает постмитохондриальная фракция печени. Разделение ее на фракцию микросом и растворимую часть значительно уменьшает нх активность. Скорость ароматического гидроксилирования существенно зависит от кофакторов. В частности, никотинамид и MgCl2 в больших количествах ингибирует реакцию. В течение 45 мин выход продукта гидроксилирования в инкубационной среде увеличивается прямо пропорционально. Гидроксилирование субстрата ингибируется SKF - 525A, HgCla. [13]
Страницы: 1