Полиядерный гидроксокомплекс
Cтраница 1
Полиядерные гидроксокомплексы образуются в разбавленных растворах в нейтральных и слабощелочных средах. По-видимому, вхождение гидроксильного иона в координационную сферу среднего комплекса Ln ослабляет координационное взаимодействие металл-лиганд и способствует размыканию части хелатных циклов монокомплекса с координацией освободившихся донорных атомов лиганда вторым ионом РЗЭ. [1]
Формирование полиядерных гидроксокомплексов обусловлено [ 13, с. [2]
Образование полиядерных гидроксокомплексов Fe ( III) не учитывается. [3]
На образование растворимых полиядерных гидроксокомплексов оказывает большое влияние присутствие посторонних анионов. В случае анионов, сильно координируемых ионами алюминия и не замещающихся гидроксид-ионами, с повышением их концентрации рН максимального осаждения гидроксида алюминия снижается. Если анионы образуют прочные связи с ионом алюминия, но замещаются гидроксид-ионом, то рН максимального осаждения А1 ( ОН) з повышается основными и снижается слабоосновными анионами. Очень прочные связи образуют ионы алюминия с рядом органических лигандов, что затрудняет протекание процесса коагуляции и требует увеличения дозы коагулянта. [4]
Установлена также величина IgA начала образования полиядерных гидроксокомплексов для различных концентраций иона родия. [5]
При добавлении основания часть А1 ( III) переходит в полиядерные гидроксокомплексы. При концентрации А1 ( 1П) более 0 3 моль / л появляется полимер А1г неизвестного состава, не содержащий АЬз в качестве фрагмента структуры. С увеличением концентрации полимера А1г образуются студни. Сетка образуется из полимера Alg, а комплексы А1Ь А12 и А1 3 находятся в ячейках сетки и не взаимодействуют с ней. Полимер Alg ведет себя как частица золя. [6]
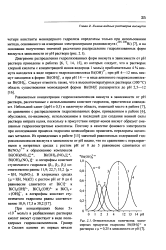 |
Относительные количества мономерных продуктов гидролиза Bi ( OH в растворах с ц 0 25 в зависимости от рН. [7] |
При концентрациях более 5х хЮ моль / л в разбавленных растворах кислот висмут существует в виде полиядерных гидроксокомплексов. [8]
Истинно растворенные формы металлов разнообразны, что связано с процессами гидролиза, гидролитической полимеризации, т.е. образованием полиядерных гидроксокомплексов, и комплексообразования с различными лигандами. [9]
По современным представлениям возможна сорбция не только простых ионных форм, но и гидролизованных катионов и даже полиядерных гидроксокомплексов I112 ], что несколько осложняет интерпретацию результатов исследований радиоколлоидного поведения радиоизотопов с помощью ионного обмена. [10]
На рис. 2.4 приведено распределение гидроксокомплексов для концентраций Bi 0 1 и 1 - 10 моль / л, из которого видно, что повышение концентрации висмута в растворе резко сдвигает равновесие в сторону образования полиядерных гидроксокомплексов. Причем в концентрированных висмутсодержащих растворах, получаемых путем растворения соединений висмута в кислородсодержащих кислотах, в области рН 0 - 1 висмут присутствует преимущественно в виде гексаядерного гидроксоком-плекса. [11]
Видно, что в обеих системах кривые для различных концентраций иона родия не совпадают друг с другом. Этот факт является прямым доказательством существования в растворах исследуемых систем полиядерных гидроксокомплексов. [12]
Соблюдение неравенств (5.17) - (5.19) позволяет создавать условия, практически исключающие образование полиядерных частиц при любых концентрациях лиганда L. Если неравенства (5.17) - (5.19) не соблюдаются, то концентрацию полиядерных частиц можно уменьшить изменением концентрации лиганда L, что часто используется для предотвращения образования полиядерных гидроксокомплексов. [13]
Из рассмотрения рис. 2 и 3 видно, что кривые образования для различных концентраций иона родия сдвинуты друг относительно друга по оси абсцисс Igft. А так как начало каждой кривой соответствует появлению в растворе гидроксокомплексов, то из представленных рис. 2 и 3 можно определить значение Igft ( при данных условиях эксперимента) начала образования полиядерных гидроксокомплексов. Данные, полученные таким образом, представлены в таблице. [14]
Галогениды ОеГ4 и 5пГ4 получают непосредственным взаимодействием простых веществ, GeCl4 образуется также при действии концентрированной НС1 на Ge02 при нагревании. В водной среде они сильно гидролизуются. При гидролизе SnCl4 образуются полиядерные гидроксокомплексы, остающиеся в растворе. Так как атом Sn имеет свободные rf - орбитали, то SnCl4 является активной кислотой Льюиса, образующей аддукты с донорами электронных пар. [15]
Страницы: 1 2