Гидроксосоли
Cтраница 2
Причем имеющиеся данные для простейших гидроксосолей не позволяют однозначно судить о структуре гидроксоаииоиа и о координационном числе центрального иона металла. В литературе описаны случаи, когда гидроксоанионы трактуются как отдельные образования, а также случаи, когда гидроксоанионы скорее можно отнести к смеси соответствующих гид-роксидов. [16]
Неорганические полимеры на основе гидроксосолей алюминия и концентрированные растворы гидроксида алюминия могут быть также использованы как вяжущие или пленки, обладающие термически устойчивыми, электроизоляционными, полупроводниковыми и другими свойствами. [17]
С разлагаются с образованием гидроксосолей переменного состава, конечный продукт разложения - МЮ. [18]
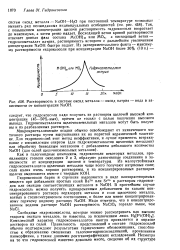 |
Растворимость в системе оксид металла - оксид натрия - вода в зависимости от концентрации NaOH. [19] |
Как и галогенидные комплексы, гидроксосоли некоторых металлов, проявляющих степени окисления 2 и 3, образуют разнотипные соединения в зависимости от концентрации щелочи и температуры. Из малоустойчивых гидроксометаллатов щелочных металлов чаще всего получают натриевые соли; соли калия очень хорошо растворимы, и из концентрированных растворов щелочи выделяются вместе с твердым КОН. [20]
Ввиду того что подавляющее большинство гидроксосолей при действии карбонатов щелочных металлов, часто присутствующих в щелочах, разлагается с образованием карбонатов, для работы нужно использовать наиболее чистые щелочи. [21]
Прежде чем описывать структуры ряда гидроксосолей, мы должны упомянуть, что некоторым из этих соединений структурные формулы были приписаны на основе предположения, что они являются координационными соединениями Вернера. [22]
Ионы ОН - в структурах гидроксосолей связаны с ионами металла, поэтому при небольшом отношении ОН: М координационная группа вокруг металла состоит в основном из атомов кислорода оксо-ионов; при увеличении отношения ОН: М доля ОН - - ионов в координационном окружении металла увеличивается. Этот процесс хорошо иллюстрируется примером гидролиза Zr ( SO4) 2 - 4H2O при 100 С до Zr2 ( OH) 2 ( SO4) 3 - 4H2O и при 200 С до Zr ( OH) 2S04, причем окружение Zr4 рассматривается в сравнении с его окружением в кубическом ZrO2, который является конечным продуктом нагревания этих солей на воздухе. [23]
Может ли гидролиз гидро - или гидроксосоли протекать более интенсивно, чем гидролиз соответствующей средней соли. [24]
Добавление солей щелочноземельных металлов к растворам гидроксосолей обычно их стабилизирует, и происходит выпадение гидроксосолей щелочноземельных металлов. [25]
При разбавлении таких растворов выпадают осадки различных гидроксосолей. [26]
Соли трехвалентного хрома легко гидролизуются, образуя гидроксосоли. [27]
При введении кислот в раствор гидроксида алюминия образуются гидроксосоли алюминия полимерного строения. [28]
Растворимость амфотерных гидроокисей в растворах щелочей е образованием комплексных гидроксосолей рассматривается в введении к 22 - й работе. [29]
Совершенно так же из электростатической теории вытекает, что гидроксосоли, являющиеся в случае трехвалентных центральных атомов довольно сильными основаниями, должны в случае четырехвалентных атомов при прочих равных условиях почти совершенно не показывать основных свойств. Как было показано выше, все эти требования вполне оправдываются на опыте. [30]
Страницы: 1 2 3