Гидролиз - амин
Cтраница 1
Гидролиз аминов с участием кислых солей сернистой кислоты протекает, очевидно, иначе, чем гидролиз под действием серной и других минеральных кислот. Это видно уже по тому, что во втором названном процессе сульфогр пни, находящиеся в мета-положении, не замедляют реакции. [1]
Гидролиз амина 33 до гидрохлорид [ 1-амино - 2 - ( 4-гидроксифенил) - 1-этил ] фосфорной кислоты 34 осуществляли в 6N водном растворе соляной кислоты при температуре 90 С в течение 28 часов. В результате целевой гидрохлорид 34 был получен и выделен с 87 % - ным выходом. [2]
Гидролиз амина до фенола протекает только в достаточно жестких условиях. В качестве гидролизующего агента предложено использовать водные растворы фосфорной кислоты. [3]
Гидролиз аминов идет в кислой среде или в присутствии солей сернистой кислоты. [4]
Гидролиз аминов с участием кислых солей сернистой кислоты протекает, очевидно, иначе, чем гидролиз под действием серной и других минеральных кислот. Это видно уже по тому, что во втором названном процессе сульфогруппы, находящиеся в мета-положении, не замедляют реакции. [5]
По другому варианту процесса циклогексиламин перерабатывается в капро-лактам с использованием стадии гидролиза амина в циклогексанон и циклогекса-нол. [6]
Сульфитная реакция аминирозання, как сказано выше, является реакцией, чбратной бисульфнтному гидролизу аминов. [7]
Сульфитная реакция аминирования, как сказано выше, является реакцией, обратной бисульфитному гидролизу аминов. [8]
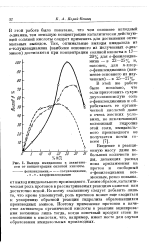 |
Выхода имидазолов в зависимости от концентрации соляной кислоты. [9] |
Таким образом, каталитическая роль протонов в рассматриваемых реакциях кажется нам достаточно ясной. Ко всему сказанному следует добавить лишь то, что кроме упомянутой, роль протонов может еще сводиться к ускорению обратной реакции гидролиза образовавшихся производных аминов. Поэтому применение протонов в качестве активатора органической кислоты в реакции ацилирова-ния возможно лишь тогда, когда конечный продукт стоек по отношению к кислотам, что, например, имеет место для случая образования имидазольных производных. [10]
Медленная стадия должна реализоваться дважды, потому что на 1 моль вновь присоединенного СО2 должны образоваться два иона НСОз; второй реагирующий моль СО2 предварительно высвобождается при регенерации карба-мат-иона. Для нейтрализации двух ионов НСОз необходимы два иона RNH, одним из которых является первично нейтрализующийся карбамин-ион, и второй получается при гидролизе амина, выделенного при регенерации карбамин-иона. [11]
Выделяющийся сернистый газ используется для подкисления раствора плава р-нафтола. Таким же путем можно получить и сс-нафтол, но в этом случае получаемый продукт недоста-точио чист. Эта реакция протекает очень легко. Гидролиз аминов ряда бензола используется редко, но амины более реакционноспособного нафталина гидролизуются легко. [12]
Выделяющийся сернистый газ используется для подкисления раствора плава р-нафтола. Таким же путем можно получить и а-нафтол, но в этом случае получаемый продукт недостаточно чист. Лучшим методом является гидролиз а-нафтиламина действием 9 2 % - ного водного раствора серной кислоты при 200 С и давлении 14 ат; при этом получается чистый продукт с выходом 94 - 95 %, Эта реакция протекает очень легко. Гидролиз аминов ряда бензола используется редко, но амины более реакционноспособного нафталина гидролизуются легко. [13]
По мнению авторов, единичный заряд в водном растворе вызывает определенную величину сжатия ( 26 см3 / моль), не зависящую от природы иона. Поэтому они не могут объяснить значительного различия в величине Дг; для гидролиза сложных эфиров и амидов. Большее отрицательное значение Д у амидов по сравнению с ацетатами, по-видимому, связано с тем, что атом азота обладает большим ван-дер-ваальсовым радиусом, чем атом кислорода, а длины связей азота и кислорода с углеродом ( или с водородом) практически - одинаковы. Поэтому образование активированного комплекса в реакциях гидролиза аминов должно сопровождаться более значительным сжатием, чем в реакциях гидролиза ацетатов. [14]
Страницы: 1