Гидролиз - ион - алюминий
Cтраница 1
Гидролиз ионов алюминия проходит еще более сложным образом. [1]
Подобным образом происходит гидролиз ионов алюминия, железа и других металлов, дающих слабые основания. [2]
При коагуляции основой процесса является гидролиз ионов алюминия и железа. Поэтому наиболее рационально вводить в обрабатываемую воду ионы этих металлов без анионов, затрудняющих в дальнейшем процессы обес-соливания. [3]
В [19, 20] приведен обзор по гидролизу ионов алюминия и железа. Методом ЯМР на протонах 17О и А1 определены числа гидратации иона A1J в водных растворах и установлен механизм гидролиза с образованием мономеров и димеров. [4]
В литературе нет точных данных о скорости гидролиза ионов алюминия в водных растворах, однако такие данные представляют интерес как для углубления знаний химии этого металла, так и для технологии получения ряда соединений алюминия. [5]
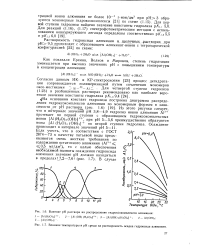 |
Влияние рН раствора на распределение гидроксокомплексов алюминия.| Влияние температуры и рН среды на растворимость осадка гидроксида алюминия. [6] |
Из этого рисунка следует, что в интервале значений рН 3 8 - 4 9 гидролиз ионов алюминия А13 протекает по первой ступени с образованием гидроксокомплексных ионов [ А1 ( Н2О) 5 ( ОН) ] 2, при рН 5 - 5 6 преимущественно образуются ионы [ А1 ( Н2О) 4 ( ОН) 2 ] по второй ступени гидролиза. [7]
Потенциометрические кривые на рис. 3 показывают, что в избытке реакционноспособного золя окиси кремния продукты гидролиза ионов алюминия вступают, главным образом, во взаимодействие с гидроксильными группами золя кремниевой кислоты, а не поли-меризуются друг с другом с образованием рыхлой гидроокиси алюминия. [8]
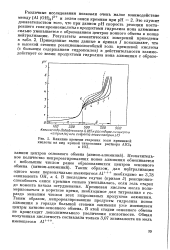 |
Влияние времени старения золя кремневой. [9] |
Это служит доказательством того, что при данном рН скорость реакции постаревшего геля кремнекислоты с продуктами гидролиза иона алюминия сильно уменьшается с образованием центров ионного обмена в конце нейтрализации. [10]
При этом не должна появляться муть или осадок, образование которых указывает на недостаток трилона в пробе и гидролиз несвязанных ионов алюминия. В этом случае следует добавить 2 - Змл трилона, снова подкислить раствор, нагреть его до кипения и нейтрализовать щелочью по фенолфталеину. Устраняя, таким образом, гидролиз алюминия, можно устанавливать необходимое количество трилона для данной пробы при неизвестном содержании алюминия. В параллельной пробе берется уже вполне определенное количество трилона ( с избытком 1 - Змл) для повторного определения алюминия и точного определения щелочности. [11]
Кривые титрования ( рис. 3) ясно указывают на то, что происходит взаимодействие гидрозоля SiCb с продуктами гидролиза ионов алюминия. [12]
На рис. 47, б приведены среднемесячные данные сорбции гумусовых веществ из днепровской воды на гидроокиси алюминия в момент ее образования при гидролизе ионов алюминия в буферной бикарбонатной среде природной воды. [13]
Подобную гидроокись алюминия наблюдали для гелей с высоким содержанием окиси алюминия, так как растворимые катионы алюминия не могут существовать в щелочных условиях и, следовательно, не могут обмениваться. Продукты гидролиза ионов алюминия, не вступающие во взаимодействие с гидрогелем окиси кремния, могли только полимеризоваться друг с другом, образуя гидроокись алюминия. [14]
Страницы: 1