Гидролиз - вещество
Cтраница 3
В некоторых работах было показано, что при гидрировании серо-органических соединений в присутствии водяных паров параллельно основной реакции протекает гидролиз серусодержащих веществ. В тех случаях, когда равновесие реакции водяного газа не достигнуто, преобладает гидрирование, но при достижении равновесия обе реакции ( гидрирования и гидролиза) протекают с приблизительно одинаковой скоростью. Активность катализатора заметно повышается при добавке водяного пара и обеспечивает практически полное удаление ( 98 %) органических сернистых соединений ( сероокиси углерода и сероуглерода) при температуре 250 С. [31]
Если, однако, и основание, и кислота, участвующие в образовании соли, очень слабы или если какое-либо из образующихся в процессе гидролиза веществ накопится в растворе в таких количествах, что станет возможным выделение его в осадок или улетучивание в виде газа, то гидролиз будет необратимым и приведет к практически полному разложению соли водой. [32]
На примере ряда соединений показана зависимость степени всасывания через кожу от химического строения и физико-химических свойств, влияния таких факторов, как температура, влажность и др. Изучены гистохимические изменения в коже и гидролиз веществ гомогенатом кожи. [33]
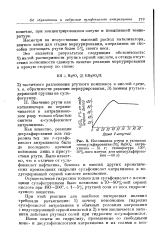 |
Поглощение ртути в условиях моносульфирования ( 5 % HgS04. антрахинона - 52 г. температура 130, 26 % - ного олеума для моносульфирования-60 г. [34] |
Осуществление гидролиза только для сульфокислот с а-стоя-щими сульфо группа ми было возможно в 70 - 80 % - ной серной кислоте при 180 - 200, с 1 - 5 % ртутной соли от веса гидролизу емого вещества. [35]
 |
График зависимости погашения от величины рН. [36] |
Наиболее важными причинами этого являются следующие: наличие в растворах анализируемых веществ посторонних ионов, изменение степени ионизации ( диссоциации) соединений, поглощающих лучистую энергию, что может повлиять на изменение окраски, а следовательно, и оптической плотности, гидролиз веществ при разбавлении растворов в ходе анализа, изменение величины рН, которое оказывает влияние на целый ряд реакций, вызывающих нарушение светопоглощения, температура раствора. Существует зависимость между величиной поглощения и рН раствора. [37]
Полученное при спектральном исследований в УФ-области отношение Е % гликозида к Е агликона, равное 0 28, характеризует исследуемое соединение как тригликозид. Гидролиз вещества эмульсином приводит к образованию лютеолин-7 - р-ру-тинозида и сахара D-глюкозы, положение которой доказано при помощи УФ-спектроскопии. Так, наличие в спектре вещества максимума при 335 лшк указывает на замещение по 4 -положению, в то время как 5 -, 7 - и З - замещенные лютеолина имеют максимум поглощения при 350 ммк. [38]
Гидролиз в паровой фазе может быть обратимым и необратимым. Механизм гидролиза веществ в газообразном состоянии зависит от химической природы исходного вещества, его реакционной способности и условий гидролиза. На практике условия гидролиза пленкообразующих соединений в парообразном состоянии подбираются так, чтобы процесс протекал необратимо. При этом одним из конечных продуктов гидролиза должно быть вещество, конденсирующееся из паров в твердом виде на поверхности обрабатываемых изделий. Гидролиз химических соединений в газообразном, состоянии в большинстве случаев происходит при относительно низких температурах. Легко гидролизуются в паровой фазе хлориды, алкоксисоединения различных элементов [22, 99, 155-157], галогенсодержащие, кремнийорганические соединения и частично замещенные алкокснсоединения с разными алкильными и арильными органическими радикалами. Все они могут осаждаться в виде тонких пленок гидроокисей. [39]
В большинстве случаев степень гидролиза невелика. Наконец, гидролиз веществ, производящихся от очень слабого основания и очень слабой кислоты, нередко протекает практически нацело. [40]
Разработан метод количественного анализа N-a - нафтилфтал-аминовой кислоты. Метод состоит в гидролизе вещества 30 % - лым едким натром и последующей отгонке с водяным паром из щелочного раствора образующегося а-нафтиламина. Амин при сочетании с диазотированной сульфаниловой кислотой образует красный азокраситель, который определяют колориметрически. По данным патента [80], реакция протекает на холоду, а при нагревании указанных веществ в качестве главного продукта получается iN - a - нафтилфталимид. [41]
Определение карбалкоксильных групп проводят в описанных выше условиях. Для отщепления карбалкоксильной группы проводится гидролиз вещества в реакционной пробирке 50 % - ным раствором КОН при 100 С в течение 40 мин. Разделение образующихся спиртов проводят на той ше колонке. [42]
ФОС, можно сделать заключение, что гидролиз изученных нами веществ протекает сравнительно медленно. Хотя в присутствии гомогената кожи гидролиз веществ ускоряется, по сравнению со спонтанным, все же периоды полураспада исчисляются сотнями часов. Следовательно, несмотря на то, что в процессе всасывания ФОИ в кожных тканях происходят реакции, направленные на их дето-ксикацию, из-за медленного течения они практического значения, по-видимому, не имеют. В кровоток вещества поступают в меньших количествах, по сравнению с теми, которые проникли в кожные ткани, но это уменьшение активного токсического агента столь несущественно, что практически не может сказываться на течении и исходе интоксикации. Однако сам факт ускорения гидролиза ФОС гомогенатом кожи подтверждает мнение о том, что во время всасывания через кожу в кожных тканях они подвергаются ферментативному расщеплению, возможны и другие превращения веществ. [43]
Такое большое различие позволяет предположить, что гидролиз вещества ( I) идет с образованием промежуточного серусодержащего циклического эфира, а при гидролизе вещества ( II) этого не происходит. [44]
Характер среды в этом случае определяется относительной силой образовавшихся кислоты и основания. Степень гидролиза, то есть отношение количества гидролизе ванного вещества к общему количеству растворенного вещества, в последнем случае очень велика. [45]
Страницы: 1 2 3