Гидролиз - силикат
Cтраница 2
Итак, скорость разрушения силикатного стекла определяется, во-первых, скоростью гидролиза силикатов поверхности и, во-вторых, скоростью диффузии воды через защитную пленку. Диффузия, в свою очередь, определяется природой пленки-плотностью ее структуры и толщиной. Наибольшая скорость гидролиза наблюдается у щелочных силикатов, далее идут силикаты некоторых двувалентных металлов-бария, свинца, кальция, магния и других. [16]
Итак, скорость разрушения силикатного стекла определяется, во-первых, скоростью гидролиза силикатов поверхности и, во-вторых, скоростью диффузии воды через защитную пленку. Диффузия, в-свою очередь, определяется природой пленки-плотностью ее структуры и толщиной. Наибольшая скорость гидролиза наблюдается у щелочных силикатов, далее идут силикаты некоторых двухвалентных металлов-бария, свинца, кальция, магния и других. Строение кремнеземной пленки определяется химическим составом тех силикатов, из которых она образовалась. Только в результате гидролиза щелочных силикатов может образоваться чисто кремнеземная пленка. При гидролизе, например, силикатов щелочных земель пленка содержит в более или менее значительных количествах и труднорастворимые гидроокиси и водные силикаты. [17]
В условиях образования силикагеля в присутствии сильного коагулятора - аммонийной соли сильной кислоты - гидролиз силиката и образование геля кремневой кислоты происходят при более высоких рН, вследствие чего скорость гидролиза уменьшается, а скорость конденсации и агрегации возрастает. Возникающая в результате гидролиза кремнекислота не успевает образовать студень, а быстро коагулирует, образуя коагель, состоящий из беспорядочно расположенных конгломератов рыхлоупакованных первичных частиц. Вторым следствием изменения соотношения скоростей стадий процесса является включение в состав геля довольно большого количества негидролизованных звеньев - кислых силикатов, что приводит к увеличению содержания катионов в осадке. [18]
Оксид бария получают кальцинированием осажденного нитрата бария или осажденного карбоната бария, а также гидролизом силиката бария. Оксид бария внешне напоминает оксид стронция, но тяжелее его ( удельный вес около 5 5) и может кристаллизоваться. Оксид бария используется при производстве гидроксида и пероксида бария, а также металлического бария. [19]
А, показывает, что образование золя SiC2 протекает в условиях сильного пересыщения и, следовательно, скорость процесса гидролиза силиката больше скорости конденсации. Дальнейшая судьба образовавшихся частиц, будут ли они расти или размер их останется без изменения, зависит от рН и температуры среды, а также продолжительности старения. Вследствие этого поверхность получаемых силикагелей достигает значительных размеров. [20]
Границах раздела концентрируются ионы гидроксила, определяемые путем электрометрического титрования, то сначала никакой адсорбции ионов гидроксила не произойдет, но ионы натрия свяжутся хемосорбцией. Впоследствии при поверхностном гидролизе силиката образуется слой ионов гидроксила. Если гель электролизуется, то при этом отмечается внезапное отклонение электрической проводимости. Первоначально она будет иметь постоянное значение, но если произойдет адсорбция, вызванная исключительно поверхностной энергией, то электрическое сопротивление должно возрасти пропорционально уменьшению в геле количества ионов. Если ионы гидроксила, адсорбированные в поверхностном слое силикагеля, только частично замещены анионами сильных неорганических кислот, то будет наблюдаться значительное изменение поверхностной активности силикагеля. Восстановление окиси серебра или его цианистой соли на силикагеле органическими восстанавливающими соединениями значительно затрудняется в присутствии ионов хлоридов, сульфатов или нитратов. Во многих случаях на геле данной коллоидной системы происходит заметно селективная адсорбция некоторых ионов. Такие явления не ограничиваются аморфными смесями гелей, например аллофанового ряда; они также широко распространены в высокодисперсных частях кристаллического материала, например в глинистых осадках. Вопросы, связанные с селективной адсорбцией, вследствие их большого значения для керамической практики и исследований почв рассматриваются ниже, - в § 275 - 320 настоящей главы А. Многие селективно-адсорбированные вещества образуют с адсорбирующим гелем адсорбционные соединения, подчиняющиеся стехиометрически определенным отношениям. Поэтому а старейшем геле, первоначально сорбирующем только поверхностью, можно увидеть все переходы от аморфного адсорбционного соединения до конечной стадии кристаллического, истинно химического соединения. Ярким примером такой последовательности химических явлений служит содержащий воду силикат бария, описанный ван Беммеленом20; этот силикат образуется из первоначального адсорбционного соединения гидрата бария с гидрогелем кремнекислоты. [21]
При действии воды щелочные соли кремневой кислоты, как кислоты слабой, легко подвергаются гидролизу с образованием свободной кремнекислоты и растворов щелочей. Довольно легко протека-кает и гидролиз силикатов щелочно-земельных металлов. [22]
При действии воды щелочные соли кремневой кислоты, как слабой кислоты, легко подвергаются гидролизу с образованием свободной кремнекислоты и растворов щелочей. Довольно легко протекает и гидролиз силикатов щелочноземельных металлов. Также подвергаются гидролизу и входящие в состав стекол более сложные кремнекислые соединения - алюмосиликаты и боросили-каты. [23]
Чтобы понять химизм разрушения стекла, рассмотрим действие на него влаги. Под действием воды происходит гидролиз силикатов щелочных металлов с образованием гидроокиси этих металлов и геля кремниевой кислоты. [24]
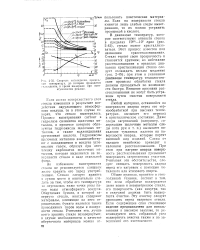 |
Скорость охлаждения, предельная температура, до которой проводится охлаждение, и время выдержки при пятиступенчатом режиме. [25] |
Процесс выветривания состоит в гидролизе силикатов щелочных металлов, в процессе которого образуются гидроокислы щелочных металлов, а также коллоидальная кремниевая кислота. Гидроокислы щелочных металлов взаимодействуют с находящимся в воздухе углекислым газом, образуя при этом пленку карбонатов щелочных металлов, которая выделяется на поверхности стекла в виде отдельной фазы. [26]
Для получения минимальной водопроницаемости желательно иметь большую поверхность твердой фазы исходного цемента и его новообразований. Гидроксид кальция, выделяющийся при гидролизе силикатов кальция в цементе, является балластом, инертным включением. [27]
 |
Химический состав эмали и водной вытяжки из нее.| Зависимость прочности сцепления от содержания в грунтовой эмали окиси кобальта. [28] |
Процесс разрушения эмалевого покрытия проявляется в потере глянца и в появлении точек ржавчины. При взаимодействии эмали с водными растворами солей происходит гидролиз силикатов. [29]
Химический состав стекла оказывает определенное влияние на величину адгезии, причем степень этого влияния в значительной мере зависит от чистоты поверхности стекла. Поскольку в результате взаимодействия с атмосферной влагой и гидролиза силикатов поверхность всех стекол покрыта тончайшими кремнеземистыми пленками и, кроме того, изменена воздействием агрессивных сред при шлифовании и полировании, то проследить влияние химического состава стекла на объемных образцах стекла почти не удается. [30]
Страницы: 1 2 3 4