Гидролиз - фторид
Cтраница 3
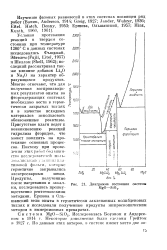 |
Диаграмма состояния системы MgO - SiO2. [31] |
Условия протекания реакций в твердом состоянии при температуре 1200 С в данных системах исследовались Фьюджай, Эйтелем ( Fujii, Eite ], 1957) и Шеллом ( Shell, 1962); последний рассматривал также влияние добавок Li20 и Na20 на характер образующихся продуктов. Многие отмечают, что для получения воспроизводимых результатов опыты во фторсодержащих системах необходимо вести в герметически закрытых тиглях и в качестве исходных материалов использовать обезвоженные реактивы. Присутствие влаги ведет к возникновению реакций гидролиза фторидов, что может повлиять на протекание основных процессов. Продукты, полученные после нагревания и закалки, исследовались преимущественно рентгеновскими методами. [32]
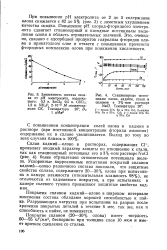
При повышении рН электролита от 2 до 5 содержание олова снижается с 82 до 5 % ( рис. 3) с заметным ухудшением качества осадка. Повышение рН хлорид-фторидного электролита сдвигает стационарный и катодные потенциалы выделения олова в область отрицательных значений. Это, очевидно, связано с адсорбцией продуктов гидролиза фторидов олова в прикатодном слое и отчасти с повышением прочности фторидных комплексов олова при понижении кислотности. [34]
Дэльман и Ланго [20] указали, что происходящее при процессе разведения смещение ионного равновесия сопровождается заметными тепловыми эффектами. Для полностью диссоциированного хлористого аммония поправка, связанная с гидролизом, имеет тот же порядок величины, что и смещение ( Д 7) при новой экстраполяции. Возможно, что тепловые эффекты, связанные с гидролизом фторидов калия и рубидия, лишь частично компенсируются смещениями Д, приведенными в табл. 121 для этих солей. В качаство примера крайней неопределенности, которая может встретиться при экстраполяции данных по теплотам разведения, зависящих от сдвига ионного равновесия, в гл. XIII, § 13, приведены значения Ь2 для серной кислоты. В этом случае Смещение, необходимое для совмещения калориметрических значений L2 теоретическими, составляет около - 450 кал. [35]
 |
Лабораторная установка. [36] |
В конце системы были расположены последовательно два платиновых дрекселя 6 для поглощения фтористого водорода, выделяющегося при гидролизе фторида алюминия. [37]
При прибавлении воды к раствору гексафторидов молибдена и вольфрама электропроводность возрастает, однако не достигает величины, отвечающей электропроводности в системе HF-ЬЬО. Это отклонение находится в прямой зависимости от концентрации фторида в растворе. Учитывая, что гексафториды молибдена и вольфрама растворяются во фтористом водороде в молекулярной форме, не образуя ионов, уменьшение электропроводности в системе может быть связано только с понижением концентрации воды вследствие проходящего процесса гидролиза фторида. [38]
Дэльман и Ланго [20] указали, что происходящее при процессе разведения смещение ионного равновесия сопровождается заметными тепловыми эффектами. В случае разбавленных растворов нейтральных солей тепловой эффект, связанный с изменением степени диссоциации воды, очень мал ( 2 кал на моль соли), однако тепловые эффекты, вызываемые сдвигом равновесия гидролиза или диссоциации таких солей, как, например, сернокислый цинк, неизвестны п могут оказаться весьма значительными. Для полностью диссоциированного хлористого аммония нопранка, связанная с гидролизом, имеет тот же порядок величины, что и смещение ( А 7) при новой экстраполяции. Возможно, что тепловые эффекты, связанные с гидролизом фторидов калия и рубидия, лишь частично компенсируются смещениями Д, приведенными в табл. 121 для этих солей. В качестве примера крайней неопределенности, которая может встретиться при экстраполяции данных по теплотам разведения, зависящих от сдвига ионного равновесия, в гл. XIII, § 13, приведены значения L2 для серной кислоты. В этом случае смещение, необходимое для совмещения калориметрических значений L2 теоретическими, составляет около - 450 кал. [39]
Для правильного выбора метода анализа гидролизованных проб необходимо знать характер протекающих гидролитических процессов. Имеющиеся в литературе сведения по гидролизу фторидов хлора нельзя считать достаточно надежными. Указывается, например, что гидролиз монофторида хлора сопровождается образованием кислорода и хлора. Одназначно отвергать возможность образования летучих соединений типа OF2 и С12 при гидролизе фторидов хлора нельзя. Однако образование их, очевидно, относится к тому случаю, когда продукты реакции сразу же выводятся из зоны реакции. [40]
Это достигается прямым переносом электронов в случае ионной связи или участием соответствующих электронов в ковалентных связях. Исходя из стабильности электронной структуры благородных газов, в течение длительного времени считали, что соединения этих газов существовать не могут. Легкость, с которой эти соединения могут быть получены, и новизна открытия, вероятно, благоприятствуют расцвету химии фтора, который, как оказалось, может нарушить стабильность замкнутых оболочек. Сразу же за первыми синтезами фторидов ксенона был получен ряд ксенон-кислородных соединений при гидролизе фторидов, а также некоторые другие галогениды. Среди других методов приготовления новых соединений здесь будет рассмотрен синтез как результат предшествующего р - распада. [41]
В отсутствие кремневой кислоты для открытия фторидов обычно служит проба травления ( ср. К тонкоизмельченному веществу добавляют концентрированную серную кислоту и осторожно нагревают в платиновом или свинцовом тигле, покрытом часовым стеклом. Освобождающийся фтористый водород обнаруживают по травлению стекла. Если же присутствует кремневая кислота ( кварц или силикаты), то выделяется фторид кремния, который на стекло не действует. Если в этом случае тигель покрыть крышкой, просверленной в середине, и положить на нее влажный черный бумажный фильтр, то в случае, если исследуемое вещество содержит фторид, на фильтре проявляется вскоре белое пятно, которое объясняется образованием гидрата двуокиси кремния в результате гидролиза фторида кремния. [42]
Для фазового анализа соединений никеля предложено несколько схем. По одной из них сначала разлагают силикаты никеля раствором фторида аммония, после извлечения силиката разлагают сульфиды никеля царской водкой. Эта схема имеет много недостатков, прежде всего не все силикаты разлагаются таким способом. Для полного разложения, например, актинолита, маложелезистых роговых обманок и других требуется повторная обработка солями. Присутствие значительных количеств сульфидов осложняет анализ, так как они разлагаются фтористоводородной кислотой. Поэтому во избежание гидролиза фторида и образования фтористоводородной кислоты необходимо иметь постоянный избыток аммиака, а в этом случае сильно замедляется разложение силикатов фторидами. Все это создает большие трудности в работе, и поэтому в последние годы эта схема почти не используется в лабораторной практике. [43]
Анализируя данные табл. 2, можно отметить, что при 50 С коррозия резко уменьшается лишь при введении 1 % NH3, а затем снова возрастает. Кроме того, при 50 С раствор, содержащий до 0 7 - 0 8 вес. Однако при 5 % NH3 на образцах опять появляется осадок. При добавлении к раствору более 2 % NH3 гидролиз фторида железа возрастает, при этом увеличивается скорость коррозии стали. [44]
Страницы: 1 2 3