Гидролиз - цирконий
Cтраница 1
Гидролиз циркония начинается при низком рН и в сильной сте-лени зависит от температуры, кислотности, концентрации циркония и других солей. [1]
Чтобы предотвратить гидролиз циркония, рекомендуется перед добавлением морина прогревать анализируемые растворы. [2]
В случае обратного титрования исключаются затруднения, связанные с гидролизом циркония, поэтому этот метод всегда предпочтителен, если необходимо анализировать чистые растворы или растворы, содержащие катионы, не мешающие определению циркония в данных условиях. При обратном титровании избытка ЭДТА рекомендуют стандартные растворы тория ( рН 2 - 3) [1087] и висмута ( рН1 - 2) [1697] с индикатором ксиленоловым оранжевым. [3]
Конечный раствор циркония в 2 М соляной кислоте не следует оставлять более чем на полчаса до добавления морина из-за возможного гидролиза циркония. Поэтому цирконий определяется отдельно в двух плавах пробы. [4]
Наиболее легко экстрагируемыми [ - излучающими продуктами деления являются цирконий и ниобий, и понижение коэффициента распределения Т - активности при понижении кислотности, вероятно, обусловливается гидролизом циркония до менее экстрагируемой формы. [5]
При низкой концентрации кислоты цирконий извлекается в виде соединений [612] типа ( Амин H) 2tZrO ( SO4) 2p -, образование которых, по-видимому, связано с гидролизом циркония. [6]
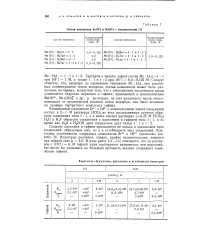 |
Состав комплексов Zr ( IV и Hf ( IV с оксикислотами. [7] |
Следует отметить, что, несмотря на одинаковое отношение Me: Н Ь при различных концентрациях ионов водорода, состав комплексов может быть различным, во-первых, вследствие того, что с уменьшением кислотности среды усиливается гидролиз циркония и гафния, приводящий к возникновению МеОН3, Me ( OH) g и др., и, во-вторых, за счет различного числа отщепляющихся от органической кислоты ионов водорода, как было показано на примере тартратного комплекса гафния. [8]
Цирконий с пирокатехиновым фиолетовым образует при рН выше 5 окрашенный комплекс ярко-синего цвета с максимумом оптической плотности 625 ммк, в то время как водный раствор самого реагента имеет максимум оптической плотности около 450 ммк и незначительно поглощает свет при 625 ммк. Прибавление комплексо-на III препятствует гидролизу циркония и не мешает развитию окраски. Только при очень большом избытке комплексона III оптическая плотность раствора заметно уменьшается. [9]
Почти все применяемые в прямых методах индикаторы образуют с ионами циркония окрашенные соединения при сравнительно низких рН 1 - 5 ( за исключением солохром фиолетового), когда возможен гидролиз циркония, вследствие чего переход окраски индикатора в точке эквивалентности становится неконтрастным. Кроме того, титрование при низких кислотностях недостаточно селективно для циркония. [10]
Процесс гидролиза солей циркония в растворах подчиняется общим закономерностям. Гидролиз галогенидов циркония прогрессирует во времени и углубляется с повышением температуры. На гидролиз циркония заметно влияет природа кислоты. [11]
Обычно в качестве экстрагентов употребляются соединения, обладающие слабокислыми свойствами, способные к образованию хелатов с экстрагируемым элементом. Таковыми являются ТТА, ацетилацетон и др. Так, Россотти [103] исследовали гидролиз индия с помощью экстракции ТТА. Далее Соловкин [ los ] при помощи этого же метода получил величины констант гидролиза циркония. [12]
Однако для этого нужно обеспечить массопередачу без сильного перемешивания. Система работает в условиях сплошной органической фазы, ситчатые пластинки изготовлены из тефлона. В таком экстракторе осуществляется очень мягкое перемешивание. Именно сочетание мягкого перемешивания, специального типа пластин, непрерывной органической фазы и кислотности позволяет разделить цирконий и гафний в присутствии значительных количеств кремнезема. Даже в отсутствие кремнезема легко образуются продукты гидролиза циркония, которые мешают процессу разделения. [13]
Гафний во всех случаях концентрируется в органическом растворителе. Присутствие небольших количеств ионов С1 - мало влияет на полноту разделения. Это позволяет практически полностью разделять цирконий и гафний при небольшом числе повторных экстракций. Для технологии метод разделения; циркония и гафния имеет то преимущество, что можно исходить из легко доступных хлоридов, полученных при обычном способе переработки руды. Повышение-концентрации роданид-ионов увеличивает коэффициенты распределения гафния и циркония, но неодинаково - первого значительно больше, чем второго, что способствует полноте разделения. Необходимую высокую концентрацию роданид-ионов создают добавлением легко растворимых в воде ЫШ § СЫ, KSCN, Ba ( SCN) 2 и др. Для успешного разделения также важно уменьшить гидролиз циркония и гафния в растворах. С целью предотвращения повышения температуры при растворении тетрахлоридов циркония и гафния производят охлаждение и перемешивание. При контакте исходного раствора с органическим растворителем большая часть ионов Н в виде HSCN переходит в органическую фазу, вследствие чего может усилиться гидролиз солей Zr ( Hf); поэтому органический растворитель предварительно насыщают HSCN до 1 - 2 N концентрации. Твердый безводный тетрахлорид циркония ( гафния) или хлорокись полученную в условиях, исключающих гидролиз растворяют в концентрированном водном растворе легко растворимого роданида и экстрагируют органическим растворителем. [14]
Страницы: 1