Гидролиз - гидрид
Cтраница 2
Различие в химической природе гидридов можно легко установить по их поведению при гидролизе. Характерной особенностью гидролиза гидридов является выделение водорода. Реакция протекает по окислительно-восстановительному, механизму. [16]
Различие в химической природе гидридов можно легко установить по их поведению при гидролизе. Характерной особенностью гидролиза гидридов является выделение водорода. Реакция протекает по окислительно-восстановительному механизму. [17]
Различие в химической природе гидридов можно легко установить по их поведению при гидролизе. Характерной особенностью гидролиза гидридов является выделение водорода. [18]
Атом кремния обладает гораздо большим сродством к кислороду, чем атом углерода. Например, SiCU моментально гидролизуется водой, тогда как ОСЬ, к воде устойчив, а растворами щелочей гидролизуется медленно. Гидролиз гидридов кремния приводит к выделению кремневой кислоты, причем дн-сплаи на воздухе самовоспламеняется, что резко контрастирует с устойчивостью соответствующих углеводородов. [19]
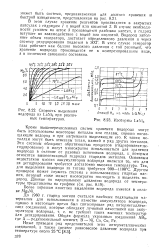 |
Скорость выделения водорода из LaNis при различных температурах. [20] |
Кроме вышеперечисленных систем хранения водорода могут быть использованы некоторые металлы или сплавы, хорошо поглощающие водород и при нагревании выделяющие его. К таким металлам могут быть отнесены титан, магний и ряд других металлов. Эти системы обладают обратимостью процессов ( гидрирование-дегидрирование) и могут многократно использоваться для хранения водорода в отличие от разовых источников водорода, к которым относится вышеописанный гидролиз гидридов металлов. Основным недостатком многих аккумуляторов водорода является то, что для их дегидрирования требуется достаточно высокая температура. Так, для выделения водорода из титана требуется 900 - 1100 С. Другим примером может служить система с использованием гидрида магния, который тоже может многократно поглощать и выделять водород. [21]
Незамещенные алкильные и арильные группы, стоящие у кремния, не реагируют с водой даже при высокой температуре. Однако этинильные группы отщепляются; углеводородные группы с большим количеством отрицательных заместителей отщепляются тем легче, чем больше этих заместителей. Кислоты и основания облегчают такое гидролитическое отщепление. Крем-нийорганические галогениды, гидриды и алкоксиды легко гидро-лизуются и гидролиз гидридов ускоряется основаниями, а гидролиз алкоксидов - кислотами. Силиламины и силазаны также гидролизуются, причем связь Si-N заменяется связью Si-О. [22]
Страницы: 1 2