Более интенсивный гидролиз
Cтраница 1
Более интенсивный гидролиз идет в присутствии больших количеств более концентрированной соляной кислоты ( сравн. [1]
Целлюлоза подвергается более интенсивному гидролизу в серной кислоте, нежели в фосфорной. [2]
Однако высокое содержание воды в щелочной целлюлозе способствует более интенсивному гидролизу монохлорацетата натрия, что приводит к уменьшению степени замещения Na-КМЦ. [3]
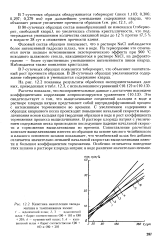 |
Кинетика накопления оксида. [4] |
Фазовый состав образцов показывает, что в растворе NaCl наблюдается более интенсивный гидролиз шлака, чем в воде. На термограмме это отмечается почти полным исчезновением экзотермического эффекта при 900 С исходного шлакового стекла, находившегося в растворе NaCl, на дифракто-грамме - более существенным уменьшением интенсивности пиков кварца. Наблюдается также появление кристаллов. [5]
Анионы А - связываются с молекулами воды водородной связью. Так, катионы элементов побочных подгрупп и непосредственно следующих за ними элементов подвергаются более интенсивному гидролизу, чем другие ионы одинаковых е ними заряда и радиуса, так как ядра первых менее эффективно экранируются d - алектронами. [6]
Соотношение количеств едкого натра, содержащегося в щелочной целлюлозе, и карбоксиметилирующего реагента должно быть по меньшей мере стехиометрическим. Такой продукт расслаивается в водных растворах, если не проводить дополнительно его нейтрализацию. Однако использование щелочной целлюлозы, содержащей значительный избыток едкого натра по отношению к монохлорацетату натрия, приводит к более интенсивному гидролизу последнего и сопровождается уменьшением степени замещения и растворимости Na-КМЦ. [7]
Гидролитическая деструкция играет существенную роль, если гидролиз потенциально оказывается основной реакцией в разрыве связей, например в полиэфирах и поликарбонатах. Атака молекулой воды может осуществиться быстро, если температура достаточно высока; эффективность атаки кислотами зависит от активности кислот и температуры. Деструкция под действием щелочных соединений определяется возможностью проникновения в полимер данного гидролитического агента: аммоний и амины могут приводить к гораздо более интенсивному гидролизу по сравнению, например, с каустической содой, поскольку последняя атакует главным образом поверхность соединения. Аморфные участки полимера подвергаются атаке быстрее всего, но и кристаллические области тоже подвергаются атаке гидролитических агентов. [8]
Анионы А связываются с молекулами воды водородной связью. Сильное воздействие анионов может привести к полному отрыву протона от молекулы Н20 - водородная связь становится ковалентной. Так, катионы элементов побочных подгрупп и непосредственно следующих за ними элементов подвергаются более интенсивному гидролизу, чем другие ионы одинаковых с ними заряда и радиуса, так как ядра первых менее эффективно экранируются ( / - электронами. [9]
Катионы связаны с молекулами воды донорно-акцеп-торной связью; донором являются атомы кислорода, имеющие две свободные электронные пары, акцептором - катионы, имеющие свободные электронные ячейки. Анионы связаны с молекулами воды водородной связью. Сильное влияние может привести к полному отрыву протона - водородная связь становится ковалентной. Так, катионы элементов побочных подгрупп и непосредственно следующих за ними элементов подвергаются более интенсивному гидролизу, чем другие ионы одинаковых с ними заряда и радиуса, так как ядра первых менее эффективно экранируются d - электро-нами. [10]
Анионы А - связываются с молекулами воды водородной связью. Сильное воздействие анионов может привести к полному отрыву протона от молекулы Н2О - водородная связь становится ковалентной. Таким образом, интенсивность взаимодействия вещества с водой определяется силой поляризующего влияния К и А на молекулы HjO. Так, катионы элементов побочных подгрупп и непосредственно следующих за ними элементов подвергаются более интенсивному гидролизу, чем другие ионы одинаковых с ними заряда и радиуса, так как ядра первых менее эффективно экранируются / - электронами. [11]
Катионы связаны с молекулами воды донорно-акцеп-торной связью; донором являются атомы кислорода, имеющие две свободные электронные пары, акцептором - катионы, имеющие свободные электронные ячейки. Анионы связаны с молекулами воды водородной связью. Сильное влияние может принести к полному отрыву протона-водородная связь становятся ковалентной. Так, катионы элементов побочных подгрупп и непосредственно следующих за ними элементов подвергаются более интенсивному гидролизу, чем другие ионы одинаковых с ними заряда и эадиуса, так как ядра первых менее эффективно экранируются d - электронами. [12]
Страницы: 1