Необратимый гидролиз
Cтраница 3
В уравнениях необратимого гидролиза ставится знак равенства. Из-за необратимого гидролиза соль A12S3 в растворе существовать не может. [31]
 |
Зависимость степени поглощения ионов кальция из раствора, содержащего избыток ионов натрия, от объема раствора. [32] |
Поскольку, однако, большинство анализов можно без труда выполнять и при комнатной температуре, часто возникает вопрос, стоит ли работать на колонке при повышенной температуре. Для растворов, склонных к необратимому гидролизу ( например, содержащих железо ( III)), следует избегать повышения температуры. Если анализируются растворы, которые легко разлагаются при комнатной температуре, то в некоторых случаях необходимо работать при пониженной температуре, чтобы избежать существенного разложения растворов. [33]
Поэтому в результате Обменных реакций между одаы-ми растворами некоторых солей е всегда образуются две новые соли. Одна из этих солей может подвергаться необратимому гидролизу с Образованием соответствующего нерастворимого основания и слабой летучей ( нераствори-юй) кислоты. [34]
Поэтому в результате обменных реакций между водными растворами некоторых солей не, всегда образуются две новые соли. Одна из этих солей может подвергаться необратимому гидролизу с образованием соответствующего нерастворимого основания и слабой летучей ( не растворимой) кислоты. [35]
Образование каких веществ в данной реакции обусловливает необратимый гидролиз. [36]
Теория равновесного связывания, согласно которой необходима обратимая гидролитическая подвижность силанолов на поверхности минерального наполнителя, позволяет предположить, что при модификации силаном границы раздела обеспечивается прочная водостойкая связь с поверхностью наполнителя. Если на каучуко-подобной, модифицированной силаном ( Поверхности раздела происходит необратимый гидролиз, то на поверхности смолы в присутствии воды образуются обратимые связи с наполнителем. [37]
При реакции с галогенами металлы IVB-группы образуют смесь продуктов с различными степенями окисления элемента. Галоге-ниды титана, циркония и гафния для высшей степени окисления являются ковалентными соединениями, которые подвергаются необратимому гидролизу. [38]
Таким образом, стадия ионизации, определяющая скорость реакции, значительно замедляется за счет обратимости процесса. При этом не обязательно, чтобы вся реакция в целом была обратима, напротив, реакция может представлять собой совершенно необратимый гидролиз; скорость реакции все больше и больше замедляется по сравнению со скоростью реакции первого порядка. Это можно выразить, видоизменив уравнение реакции Зк1 - типа при условии постоянной активной массы замещающего агента. [39]
Гидролиз их значительно усиливается при нагревании и приводит к образованию осадков гидроксосолей. Что же касается солей этих металлов, образованных другими одноосновными кислотами, таких, как нитриты, гипохлориты, гипобромиты, - то практически эти соли не выделены вследствие полного и необратимого гидролиза. [40]
Как правило, реакции, сопровождающие распределение неорганических соединений между двумя фазами, являются быстрыми. В большинстве случаев при низкой общей скорости массопередачи она определяется реакцией в водной фазе. Примером является реакция необратимого гидролиза металла в водном растворе, или медленная реакция внутренней перестройки комплексов, таких, как нитратные комплексы нитрозилрутения. В таких системах распределение зависит от истории водного раствора, так как его определяют фактически в неравновесных условиях. [41]
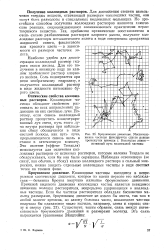 |
Броуновское движение. Местоположение частицы фиксируется спустя равные промежутки времени t. Волнистая линия - истинный путь коллоидной частицы. [42] |
Наиболее удобен для демонстрации коллоидный раствор гидрата окиси железа. Для его получения в кипящую воду по каплям прибавляют раствор хлорного железа. Соль подвергается при этом необратимому гидролизу, и получается коллоидный раствор в виде жидкости интенсивно бурого цвета. [43]
Наиболее удобен для демонстрации коллоидный раствор гидрата окиси железа. Для его получения в кипящую воду по каплям прибавляют раствор хлорного железа. Соль подвергается при этом необратимому гидролизу, и получается коллоидный раствор гидрата окиси железа в виде жидкости интенсивно бурого цвета. [44]
В лабораторной практике обычно процесс гидролиза проводят в открытых системах. При нагревании раствора сульфида аммония растворимость аммиака и сероводорода в воде уменьшается, они уходят из сферы реакции, и равновесие процесса резко смещается вправо. Гидролиз, сопровождающийся уходом продуктов реакции из зоны реакции или образованием осадка, часто условно называют необратимым гидролизом ( не в термодинамическом смысле. [45]
Страницы: 1 2 3 4