Более глубокий гидролиз
Cтраница 2
С помощью универсального индикатора измеряют рН 0 1 М растворов РеСЬ и FeCU. В каком растворе протекает более глубокий гидролиз и почему. [16]
Равным образом казеин, предварительно гидролизованный химотрипсином, гидролизуется дальше добавленным трипсином. В некоторых случаях химотрипсин производит даже более глубокий гидролиз белка, чем трипсин, и при этом расщепляется почти половина пептидных связей в белковой молекуле. [17]
Связь Zr с ОН-ионами прочнее, чем с Cl-ионами, поэтому вытеснение последних при взаимодействии циркония с ксиленоловым оранжевым происходит легче. Нагревание раствора соли циркония при невысокой кислотности до прибавления реагента приводит к более глубокому гидролизу, и оптическая плотность для предварительно нагретых растворов несколько ниже, чем для ненагретых. Нагревание растворов с концентрацией циркония 1 10 - 3 М и рН; 2 перед добавлением реагента приводит к полной потере, реакционной способности циркония. [18]
Полимерные формы довольно легко разрушаются многими комплексообразователями, как фторид, перекись водорода, иногда - оксалат и др. Однако крупные анионы металлохром ных индикаторов очень медленно реагируют с полимерными гидролизованными формами высоковалентных ионов. Стояние или нагревание раствора не ускоряет образования окрашенного комплекса, так как при этом еще быстрее идет более глубокий гидролиз. При длительном стоянии или нагревании гидролиз становится, кроме того, менее обратимым. [19]
Строение пенициллина было установлено при помощи реакций гидролиза. Как уже отмечалось выше, пенициллин крайне легко, главным образом в кислой среде, гидролизуется, в результате чего расщепляется характерное р-лактамное кольцо этих веществ. Более глубокий гидролиз гладко приводит к получению так называемого пенициламина ( тиоаминокислоты) наряду с пеналъдовой кислотой ( ( 3-аль-дегидокислотой); последняя в результате декарбоксилирования мгновенно превращается в пениллоальдегид. [20]
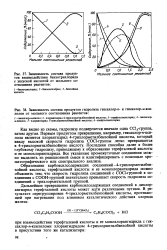
Как видно из схемы, гидролизу подвергается вначале одна СС13 - группа, затем другая. Первым продуктом превращения, например, гексахлор-п-кси-лола является хлорангидрид 4-трихлорметилбензойной кислоты, который ввиду высокой скорости гидролиза COCl-группы легко превращается в 4-трихлорметилбензойную кислоту. Последняя способна далее к более глубокому гидролизу, приводящему к образованию терефталевой кислоты и ее монохлорангидрида. [22]
Он относится к группе протеолитических ферментов. Подобно трипсину, он гидролизует белки и пептоны с образованием относительно низкомолекулярных пептидов. В некоторых случаях химотрипсин производит более глубокий гидролиз белка, чем трипсин. Отличается также от трипсина тем, что вызывает свертывание молока, в то время как трипсин свертывания молока не вызывает. Химотрипсин более стоек, чем трипсин, и медленнее инактивируется. [23]
К 15 - 20 мл клейстера в стаканчике или в колбочке добавляют 1 мл разбавленной серной кислоты и кипятят смесь 5 - 10 мин, при этом через каждые 1 - 2 мин отливают в отдельную пробирку немного ( 1 - 2 мл) горячей жидкости, быстро охлаждают пробу в воде, добавляют каплю раствора иода и ставят пробирку в штатив. Последовательные пробы обнаруживают постепенное изменение окраски при реакции с иодом. Это происходит в результате все более глубокого гидролиза крахмала и первоначально образующихся декстринов. [24]
Сначала адсорбируются и феноляты, но их количество по сравнению с общим количеством фенолятного щелока чрезвычайно мало. Однако это количество увеличивается, если активированным углем очищаются феноляты, содержащие также высококипящие фенолы. Можно предположить, что это связано с более глубоким гидролизом этих фенолятов. В этом случае возрастает расход активированного угля на очистку и очистка менее удовлетворительная. [25]
При инверсии щелоков ( кипячение Зчас, концентрация серной кислоты 4J &) обнаружилась зависимость, специфичная только для бисульфитвых варок. Как при варке осины, так и березы увели - чение выхода целлюлозы сверх 5 - 55 % приводит к возрастанию количества РВ после инверсии. Это указывает, что при биоульфия-ной варке целлюлозы высокого выхода ( ЦВВ) по мере снижения выхода целлюлозы, т.е. с усилением агрессивности обработки наряду с более глубоким гидролизом гемицеллюлоз опережающе возрастает окисление образующихся моносахаридов. [26]
Физические свойства камеди вишни близки к свойствам камеди сливы. Камедь вишни содержит повышенное количество пентозанов по сравнению с камедями сливы. При мягком гидролизе удаляются все пентозаны и получается продукт, имеющий такой же состав, как частично деполимеризован-ные камеди сливы. При более глубоком гидролизе образуется альдобионовая кислота, идентичная с альдобионовой кислотой камеди сливы. Повидимому, камедь вишни имеет строение, подобное строению камеди сливы, но окончательно этот вопрос остается еще не выясненным. [27]
Ферментный комплекс ксилоаваморин удаляет из образцов целлюлоз 3 - 8 % ксилана, а из холоцеллюлозы - около 15 % ксилана от его первоначального количества. Под действием ксилоаваморина у образцов сульфатных целлюлоз снижается степень полимеризации, а у сульфитных этого не наблюдается. Если те же образцы [11] обрабатывают ферментным комплексом целлолигнорпна ( содержит гемицеллюлазы и целлюлазу) и потери массы при этом составляют 5 8 - 11 4 % у сульфатных, 4 8 - 7 5 % у сульфитных целлюлоз и 9 8 % у холоцеллюлозы, то из образцов целлюлоз удаляется 6 - 17 %, а из холоцеллюлозы - 26 % ксилана от его первоначального количества. Это свидетельствует о том, что более глубокий гидролиз ксилана возможен только при частичной деградации собственно целлюлозы. [28]
Кристаллический химотрипсин, подобно трипсину, гидролизирует как белки, так и пептоны с образованием относительно низкомолекулярных пептидов. Он расщепляет по преимуществу те пептидные связи, на которые трипсин не действует. Это следует из того, что если на казеин воздействовать трипсином, а затем, по окончании триптического гидролиза добавить химотрипсин, то гидролиз белка продолжается. Равным образом казеин, предварительно гидролизованный химотрипсином, гидролизуется дальше добавленным трипсином. В некоторых случаях химотрипсин производит даже более глубокий гидролиз белка, чем трипсин, и при этом расщепляется почти половина пептидных связей в белковой молекуле. [29]
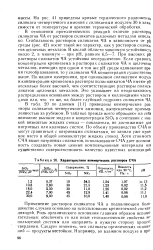 |
Характеристики коммерческих растворов СЧА. [30] |
Страницы: 1 2 3