Гидроокись - калий
Cтраница 1
 |
Значение калия для сельского хозяйства. [1] |
Гидроокись калия, едкое кали КОН - твердое белое вещество, лучше растворимое в воде, чем едкий натр. Раствор едкого кали окрашивает синий лакмус в красный цвет, а фенолфталеин - в малиновый. Едкое кали и его концентрированные растворы разрушают растительные и животные ткани. [2]
Гидроокись калия для кумаринов. [3]
Гидроокиси калия, алюминия и магния, взятые в качестве исходных веществ, обусловливают образование различающихся по характерным признакам синтетических монтмориллонитов; в различных природных месторождениях они образуют кристаллические растворы глиноземистых и магнезиальных монтмориллонитов ( см. А. [4]
Гидроокись калия, так же, как гидроокись натрия, является едким веществом, действующим на кожу и слизистые оболочки прижигающим образом. Особенно опасно попадание даже малейших количеств щелочи в глаза. [5]
Гидроокись калия ( едкое кали) КОН - твердое вещество белого гвета ( плотность 2 0 г / см3, г. пл. Хорошо растворима в воде. Едкое кали используют в качестве катализатора в производстве кремнийорганических лаков и высоковязких жидкостей ПМС. [6]
Гидроокись калия ( едкое кали), КОН, получают подобно гидроокиси натрия, в частности электролизом водного раствора хлорида калия в электролитической ячейке с ртутным катодом. [7]
Гидроокись калия применяется потому, что, являясь одним из продуктов катодной реакции, она воспроизводится в процессе измерения, что позволяет поддерживать стабильность показаний отсчета. Этот фактор приобретает особое значение при работе с малым объемом электролита. Электроды с гидроокисью калия имеют малое время разогрева. Добавление гидроокиси при сборке электрода нивелирует его рабочую характеристику, создавая условия, аналогичные складывающимся после длительного периода эксплуатации. [8]
Гидроокись калия следует предпочесть гидроокиси натрия, так как натриевые соли могут при титровании образовывать эмульсии. Растворителем может служить также метанол или нормальный амиловый спирт, но первый имеет низкую температуру кипения, а второй смешивается с водой не во всех отношениях. [9]
Гидроокись калия КОН - ценное сильнощелочное вещество, обладающее свойствами, аналогичными свойствам гидроокиси натрия. [10]
Гидроокись калия КОН ( едкое кали), как и едкий натр - очень сильное основание, еще больше растворимое в воде, чем NaOH. Применяется для получения жидких калийных мыл. Кроме того, раствор КОН используется как электролит в щелочных аккумуляторах ( стр. [11]
Гидроокись калия реактивной чистоты получают аналогично гидроокиси натрия. Свежие калиевые щелоки после амальгамного электролиза отстаивают в течение нескольких дней, фильтруют через ватные фильтры и упаривают в никелевых плавильных котлах до получения прозрачного и светлого расплава, что обычно достигается при 400 - 420 С. [12]
Сколько гидроокиси калия ( в молях) можно получить в результате гидролиза этилата калия и какова концентрация полученного раствора гидроокиси, если его объем равен 75 мл. [13]
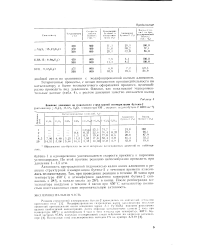 |
Влияние давления на показатели структурной изомеризации бутена-2. [14] |
Активность протравленной гидроокисью калия окиси алюминия в реакции структурной изомеризации бутена-2 с течением времени изменялась незначительно. Гак, при проведении реакции в течение 10 часов при температуре 450 С и атмосферном давлении конверсия бутеиа-2 снижалась с 28 % в начале опыта до 26 % в конце. После регенерации катализатора воздухом в течение 4 часов при 450 С катализатор полиостью восстанавливал свою первоначальную активность. [15]
Страницы: 1 2 3 4