Гидроокись - медь
Cтраница 2
Гидроокись меди нерастворима в воде, но растворима в водном рас-творе аммиака. [16]
Гидроокись меди растворяется в сахарах, как в многоатомных спиртах, давая синее окрашивание. [17]
Гидроокись меди легко растворяется в разбавленных кислотах и аммиаке. [18]
Гидроокиси меди, кадмия и серебра легко растворяются в растворе аммиака с образованием комплексных соединений. [19]
Гидроокиси меди и кадмия и окись серебра растворяются в избытке раствора аммиака с образованием аммиакатов; [ Cu ( NHs) 4 ] - интенсивного синего цвета, остальные - бесцветны. Реакции катионов IV аналитической группы с NH4OH широко используют в систематическом ходе анализа катионов. [20]
Гидроокись меди частично растворяется также в избытке концентрированного раствора щелочи, образуя неустойчивые соли, называемые купритами. [21]
Гидроокись меди существует в двух структурах - аморфной и кристаллической. Аморфная структура образуется при очень осторожном осаждении раствором щелочи из какой-либо соли меди в виде синего осадка - геля, который после высушивания переходит в гидрат с переменным содержанием воды. [22]
Гидроокись меди промывают декантацией, причем с целью ускорения процесса первые промывки проводят при 40 - 45 С; осадок фильтруют на нутч-фильтре. [23]
Гидроокись меди, получаемая по этому методу, занимает меньший объем и значительно лучше отстаивается и фильтруется, что позволяет ускорить процесс производства. [24]
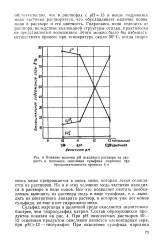 |
Влияние величны рН исходного раствора на скорость и механизм окисления сульфида марганца при продолжительности процесса 6 ч. [25] |
Гидроокись меди отделить от раствора, вследствие коллоидной структуры осадка, практически не представляется возможным. [26]
Гидроокись меди, 5 % - ный раствор в 20 - 25 % - ном растворе аммиака. [27]
Гидроокись меди, являющаяся бифункциональным соединением реагирует одновременно с двумя гидрбксильными группами целлюлозы. [28]
Гидроокись меди легко разлагается даже под водой при осторожном нагревании, превращаясь в черную окись меди. [29]
Гидроокись меди является окислителем. [30]
Страницы: 1 2 3 4