Гидроокись - металл - группа
Cтраница 1
Гидроокиси металлов I группы и подгруппы бария II группы представляют собой растворимые в воде, бесцветные, горькие на вкус твердые вещества, не имеющие запаха. Водные растворы 98 щелочей на ощупь скользкие. [1]
Хотя все гидроокиси металлов III группы практически не растворимы в воде, однако величины произведений растворимости их все же различаются весьма сильно. Указанное различие сказывается, например, при действии: на катионы III группы аммиаком в присутствии солей аммония. [2]
Активными катализаторами являются окиси и гидроокиси металлов II группы. В табл. 7 приведены рассчитанные по данным [280-282, 659] величины чисел активных центров на 1 см2 поверхности гидроокисей и скорости реакции, отнесенные к одному активному центру. [3]
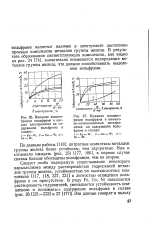 |
Влияние концентрации вольфрама в кислых электролитах на содержание вольфрама в сплаве.| Влияние концентрации вольфрама в аммиач-но-лимоннокислых электролитах на содержание вольфрама в сплаве. [4] |
Следует особо подчеркнуть существование некоторого параллелизма между растворимостью гидроокисей металлов группы железа, устойчивостью их оксикислотных комплексов [117, 118, 227, 221] и легкостью осаждения вольфрама в их присутствии. [5]
Из изложенного следует, что относительно невысокие поверхности гидроокисей металлов II группы обусловлены легкой кристаллизуемостью этих веществ, вследствие чего наряду с образованием первичных частиц имеет место ориентировочное срастание монокристалликов. Конечный размер поверхности определяется степенью срастания. Последняя возрастает с увеличением содержания продуктов неполного гидролиза. [6]
Упомянутые выше рекомендации относятся, главным образом, к композициям, в которых в качестве загустителя используются окиси и гидроокиси металлов II группы. [7]
Экстракцию проводят в присутствии цианида, который связывает в комплексы элементы группы цинка, и в присутствии цитрата, предупреждающего осаждение гидроокисей металлов группы аммиака. В этих условиях мешают только: олово ( II), таллий ( I) и висмут. Мешают окислители; их надо восстановить добавлением гидроксиламина. [8]
Несмотря на то что процессу каталитического распада газообразного озона посвящено немало работ, в большинстве случаев полученные результаты носят качественный характер. В ранней работе Маншо [30] отмечается, что разложение озона ускоряют такие металлы, как Pt, Pd, Ru, Cu, W и др. Каталитическое действие металлов на разложение озона ( 0 5 - 1 5 %) при 100 изучали Каштанов с сотрудниками [31], отметившие высокую активность серебра и сравнительно слабую активность Си, Pd, Sn. К числу наиболее полных работ по катализу озона нужно отнести работу Шваба [32], который провел исследование каталитических свойств окислов и гидроокисей металлов I-IV групп по отношению к озону. [9]
Страницы: 1