Гидроокись - трехвалентный металл
Cтраница 2
Кроме того, не всегда бывает нужно производить полный анализ этих минералов. Если, как это часто случается, не требуется определение магния, то можно выделять кальций без предварительного отделения гидроокисей трехвалентных металлов. Определение алюминия Р таком случае целесообразно производить объемным способом в фильтрате, полученном после выделения кремневой кислоты. [16]
Эти системы были приготовлены совместным осаждением едким натром из смеси растворов соответствующих хлоридов. При исследовании выяснилось, что слоистая гексагональная решетка построена из упорядоченных слоев Mg ( OH) 2, между которыми располагаются неупорядоченные слои гидроокисей трехвалентных металлов, причем каждый четвертый слой повторяет первый. Гидроокиси с такой структурой названы [21, 22] двойными гидроокисями или двойными слоистыми структурами, а состав их условно обозначен индексом M4Aj, где М означает гидроокись магния, а А - гидроокись алюминия. С увеличением ионного радиуса катиона ( от 0 57 А для А13 до 0 67 А для Fe3) элементарная ячейка по оси с несколько сжимается, а по оси а расширяется. [17]
Эти системы были приготовлены совместным осаждением едким натром из смеси растворов соответствующих хлоридов. При исследовании выяснилось, что слоистая гексагональная решетка построена из упорядоченных слоев Mg ( ОН) 2, между которыми располагаются неупорядоченные слои гидроокисей трехвалентных металлов, причем каждый четвертый слой повторяет первый. Гидроокиси с такой структурой названы [21, 22] двойными гидроокисями или двойными слоистыми структурами, а состав их условно обозначен индексом M. С увеличением ионного радиуса катиона ( от 0 57 А для А13 до 0 67 А для Fe3) элементарная ячейка по оси с несколько сжимается, а по оси а расширяется. [18]
Кроме ионов, образующих с ионами осадка труднорастворимые или малодиссоциирующие соединения, осадки могут также адсорбировать ионы водорода и особенно сильно ионы гидроксила. В последнем случае осадок будет сильно загрязняться щелочами. С этим необходимо считаться, например, при получении гидроокисей трехвалентных металлов. [19]
Раствор выпаривают досуха, прибавляют 3 мл НС1 ( пл. Почти сухой остаток растворяют в ра.зб. НС1, вводят 4 мл H2SO4 ( 1: 1) и нагревают до выделения паров серной кислоты. Далее осаждают 25 % - ным раствором аммиака гидроокиси трехвалентных металлов, фильтруют, промывают осадок 1 % - ным раствором NH4C1, содержащим аммиак, растворяют в 3 5 М H2SO4, переносят в мерную колбу емкостью 100 мл и разбавляют до метки серной кислотой той же концентрации. [20]
Раствор выпаривают досуха, прибавляют 3 мл НС1 ( пл. Почти сухой остаток растворяют в ра.зб. HQ, вводят 4 мл H2S04 ( 1: 1) и нагревают до выделения паров серной кислоты. Далее осаждают 25 % - ным раствором аммиака гидроокиси трехвалентных металлов, фильтруют, промывают осадок 1 % - ным раствором NH4C1, содержащим аммиак, растворяют в 3 5 М H2S04, переносят в мерную колбу емкостью 100 мл и разбавляют до метки серной кислотой той же концентрации. [21]
При рассматривании перла под микроскопом можно заметить мелко раздробленный металл, суспендированный в бесцветном стекле. В присутствии никеля бумага окрашивается в зеленоватый цвет ( - при очень малом количестве никеля бумага бесцветна) или в синеватый при наличии также и обальта. Если теперь пятно смочить едким натром или кали и подвергнуть его действию паров брома ( выделяемых из широкогорлой склянки при взбалтывании в ней небольшого количества, бромной воды), то в присутствии никеля или кобальта образуется черное пятно, обусловленное образованием гидроокиси трехвалентного металла ( стр. Часто почернение вначале не происходит; в этом случае бумагу смачивают еще раз едким кали и снова обрабатывают бромом. На этот раз пятно, если никель присутствует, окрасится в черный цвет. [22]
При рассматривании перла под микроскопом можно заметить мелко раздробленный металл, суспендированный в бесцветном стекле. В присутствии никеля бумага окрашивается в зеленоватый цвет ( при очень малом количестве никеля бумага бесцветна) или в синеватый при наличии также и кобальта. Если теперь пятно смочить едким натром или кали и подвергнуть его действию паров брома ( выделяемых из широкогорлой склянки при взбалтывании в ней небольшого количества, бромной воды), то в присутствии никеля или кобальта образуется черное пятно, обусловленное образованием гидроокиси трехвалентного металла ( стр. Часто почернение вначале не происходит; в этом случае бумагу смачивают еще раз едким кали и снова обрабатывают бромом. На этот раз пятно, если никель присутствует, окрасится в черный цвет. [23]
Действие кислоты на алюминий дает пример анодного контроля; в этом случае коррозия концентрируется на уязвимых точках окисной пленки, которая на других участках является непроводящей. ОН) начнут играть определенную роль в анодной реакции. Скорость коррозии алюминия определяется в основном присутствием ионов, которые могут проникать через пленку. Соляная кислота - поэтому растворяет алюминий гораздо скорее, чем серная. Это также связано со способностью реагентов переводить в раствор или в коллоидальное состояние анодно образованную гидроокись алюминия; это объясняет, почему в разбавленном растворе гидроокиси натрия алюминий корродирует гораздо быстрее, чем в разбавленных кислотах. Это, возможно, связано с тем фактом ( известным всякому лабораторному работнику, пытавшемуся очистить стеклянную посуду после ее употребления при исследовании процессов коррозии), что разбавленная соляная кислота неспособна практически растворять пленки гидроокисей трехвалентных металлов, а концентрированная - растворяет их в течение нескольких секунд. [24]
Наибольшее значение имеет ализарин. Ализарин в смеси с пурпурином и пурпуринкарбоновой кислотой находится в виде глюко-зида в корнях марены. Дл я производства пигментов применяют преимущественно ализарин. Он представляет собой порошок тускло-желтого цвета, в воде нерастворим, в спирте растворяется при нагревании. Ализарин содержит две гидрокси - и две кетогруппы. Гидроксигруппы обладают кислыми свойствами, способны к образованию солей с солями одно - и двухвалентных металлов; кетогруппы способны прочно связывать атомы металлов за счет дополнительных валентностей. С гидроокисями трехвалентных металлов ализарин образует адсорбционные соединения за счет как гидрокси -, так и кетогрупп. [25]
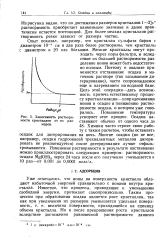 |
Зависимость растворимости кристаллов от их размеров. [26] |
Опыт показал, например, что кристаллы сульфата бария с диаметром 10 - 4 см в два раза более растворимы, чем кристаллы с диаметром в 20 оаз большим. Мелкие кристаллы могут проходить через поры фильтра, и вследствие их большей растворимости разделение ионов может быть недостаточно полным. Поэтому в анализе применяется отстаивание осадка в маточном растворе ( так называемое ди-герирование), часто сопровождаемое еще и нагреванием на водяной бане. Повышение температуры ускоряет этот процесс. Химики часто строят свою работу с таким расчетом, чтобы оставлять осадок для дигерирования на ночь. Многие осадки ( но не все; например, осадки гидроокисей трехвалентных металлов дигери-ровать не рекомендуется) после дигерирования лучше отфильтровываются. [27]
Страницы: 1 2