Гидроокись - щелочной щелочноземельный металл
Cтраница 2
Необходимая величина рН среды достигается применением водорастворимых оснований - гидроокисей щелочных и щелочноземельных металлов, а также солей, образованных слабыми кислотами и аммонием или щелочными и щелочноземельными металлами. Могут быть применены также органические основания - алифатические амины или их соли со слабыми кислотами. Обычно применяются 1 - 10 % - ные водные растворы указанных соединений. [16]
На практике к щелочам относят более широкий круг химических товаров-окиси и гидроокиси щелочных и щелочноземельных металлов и сложных радикалов, а также углекислые соли щелочных металлов, поскольку растворы последних вследствие гидролиза имеют щелочную реакцию. [17]
Получение резолов проводят в водном растворе в присутствии различных катализаторов - гидроокисей щелочных и щелочноземельных металлов, NH3, первичных и вторичных аминов. Резолы, хорошо растворимые в воде, получают при умеренном избытке формальдегида ( 1: 1 1 - 1 3) при температуре ниже 60 С и высокой концентрации щелочи. При этом образуются низкомолекулярные олигомеры с высоким содержанием свободного фенола. С повышением температуры реакции растворимость олиго-меров в воде уменьшается. При получении резолов по двухстадийной технологии [191 ] сначала из фенола и формальдегида ( в соотношении 1: 0 8) в присутствии оснований или кислот получают новолаки, которые затем превращают в резолы, содержащие СН2ОН - группы, взаимодействием с избытком формальдегида. [18]
На практике к щелочам относят более широкий круг химических веществ - окиси и гидроокиси щелочных и щелочноземельных металлов и сложных радикалов, а также углекислые соли щелочных металлов, поскольку их растворы вследствие гидролиза имеют щелочную реакцию. [19]
В сточной воде одновременно могут присутствовать либо бикарбонаты и карбонаты, либо карбонаты и гидроокиси щелочных и щелочноземельных металлов. [20]
Реже применяется гидролиз под действием оснований, который в относительно мягких условиях ( растворы гидроокисей щелочных и щелочноземельных металлов, соды, бикарбоната) приводит к разрыву лишь некоторых типов гликозидных связей ( см. гл. Этим путем также трудно получить фрагменты, содержащие узловую гликопептидную связь; существенно, однако, что именно некоторые типы такой связи чувствительны к подобным воздействиям. Это в особенности относится к О-гликозидной связи и, очевидно, к слож-ноэфирной и О-ацилгликозидной связям. Распад под действием оснований в сочетании с кинетическими или полукинетическими измерениями используется сейчас для доказательства наличия О-гликозидной связи в гликопротеинах18 38 и в будущем позволит, по-видимому, создать один из методов их избирательного гидролиза. В последнее время широко используется гидролиз разбавленными растворами щелочей в присутствии небольших количеств NaBH438 39 40; в этом случае концевые восстанавливающие моносахаридные остатки отщепляюдихся олигосахаридов восстанавливаются, что предохраняет их от деструкции под действием щелочи и дает возможность выделить и подвергнуть исследованию. [21]
II) из дихлорбутена ( I) в качестве омыляющего агента нами были исследованы водные растворы гидроокисей щелочных и щелочноземельных металлов, соли слабых кислот и сильных оснований, а также вода. Омыление дихлорбутена ( I) даже 1 % раствором гидроокиси натрия приводит к образованию твердого полимера. Однако, если раствор гидроокиси натрия вводить постепенно и, что особенно важно, поддерживая в системе значение рН постоянным и равным 7, можно получить изомерные бутендиолы с выходом 40 % при полной конверсии исходного дихлорбутена. [22]
Вернер чрезвычайно обобщил это представление, распространив его не только на гидроксо-соединения, но также и на гидроокиси щелочных и щелочноземельных металлов. [23]
Вернер чрезвычайно обобщил это представление, распространив его не только на гндроксо-соединения, но также и на гидроокиси щелочных и щелочноземельных металлов. [24]
Это представление, справедливое для гидроксосоединений тяжелых металлов, было совершенно произвольно обобщено Верне-ром и распространено на гидроокиси щелочных и щелочноземельных металлов, хотя между гидроксосоединениями металлов восьмой группы и гидроокисями МОН и М ( ОН) 2 ( где М - щелочной или щелочноземельный металл) существует принципиальная разница. В силу этого, а также некоторых других обстоятельств положения Вернера об ангидрокислотах, аквакислотах, ангидро - и акваоснованиях вскоре было оставлено. [25]
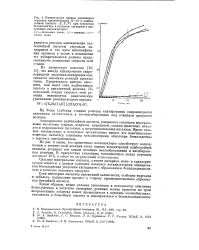 |
Кинетические кривые накопления перекиси ацетилбензоила ( 1 - 3 и надбен-зойной кислоты ( Г, 2, 3 при окислении бензальдегида в уксусном ангидриде в присутствии катализаторов. [26] |
Ацилирование надбензойной кислоты ускоряется сильными минеральными кислотами ( серная, хлорная), пиридином, солями щелочных металлов и гидроокисями щелочных и щелочноземельных металлов. Кроме сильных минеральных и некоторых органических кислот все перечисленные вещества являются хорошими катализаторами окисления бензальдегида в перекись ацетилбензоила. [27]
Дибром -, 1 2-дифтор -, 1 2-дииоднитроэтаны в присутствии основных катализаторов ( карбонаты и гидрокарбонаты щелочных металлов, гидроокиси щелочных и щелочноземельных металлов, третичные амины), отщепляя галогеноводороды, превращаются в галогенонитрополимеры. [28]
Для лолучения диола ( II) из дихлорбутена ( I) в качестве омыляющего агента нами были исследованы водные растворы гидроокисей щелочных и щелочноземельных металлов, соли слабых кислот и сильных основа-кий, а также вода. Омыление дихлорбутена ( I) даже 1 % раствором гидроокиси натрия приводит к образованию твердого полимера. Однако, если раствор гидроокиси натрия вводить постепенно и, что особенно важно, поддерживая в системе значение рН постоянным и равным 7, можно долучить изомерные бутендиолы с выходом 40 % при полной конверсии исходного дихлорбутена. [29]
В умеренных условиях ( температура около 70 С), при избытке формальдегида ( 1 5 - 2 моля на 1 моль фенола) и соответствующих количествах гидроокисей щелочных и щелочноземельных металлов образуются относительно низкомолекулярные, водорастворимые смолы, содержащие преимущественно метилольные группы. В их состав входят различные одно - и двухядерные фенолоспирты с высоким содержанием метилольных групп ( обладающие поэтому высокой реакционной способностью), свободные фенол и формальдегид. [30]
Страницы: 1 2 3