Гидроокись - натрий
Cтраница 3
Гидроокись натрия используется при производстве искусственного шелка, мыла, бумаги, взрывчатых веществ, красителей и других химических соединений. Это вещество также применяется для очистки металлов, электролитической экстракции цинка, лужения, стирки и отбеливания. Тринатрий фосфат находит применение в фотографических проявителях, в смесях детергентов и в бумажной промышленности, используется для очистки сахара, удаления накипи, смягчения воды, стирки и дубления кожи. Тринатрий фосфат также используется для очистки воды и в качестве эмульгатора при производстве сыра. Динатрий фосфат входит в состав удобрений, фармацевтических препаратов, керамики и детергентов. Он используется для утяжеления шелка, окраски и нанесения рисунка в текстильной промышленности, а также для огнестойкой пропитки древесины и бумаги. Он также служит добавкой к пищевым продуктам и дубильным средством. Гипохлорит натрия применяется при отбеливании в текстильной и целлюлозно-бумажной промышленности. Он применяется для дезинфекции стекла, керамики и воды, а также как дезинфицирующее средство в плавательных бассейнах. Хлористый натрий используется для обработки металлов, обработки шкур, удаления льда с дорог и для консервации пищевых продуктов. Он также находит применение в фотографии, в производстве химикатов, керамики и мыла, в ядерных реакторах. [31]
Гидроокись натрия, тринатрийфосфат и карбонат натрия выпускаются промышленностью в виде твердых веществ с нормируемыми показателями основного вещества в продукте, что позволяет приготовить их водные растворы с достаточной точностью. [32]
Гидроокиси натрия и калия являются энергичными плавнями, но редко применяются в полном анализе горных пород, потому что даже лучшие продажные препараты едких щелочей не так чисты, как карбонат и бикарбонат натрия; кроме того, для сплавления с едкими щелочами приходится применять серебряные и золотые тигли вместо платиновых; тигли из этих металлов не допускают применения таких высоких температур, при которых проводят сплавления в платиновой посуде; хотя золотые и серебряные тигли разрушаются меньше, чем платиновые, все же значительное количество металла переходит в плав и должно быть затем удалено. [33]
Гидроокись натрия ( едкий натр, каустическая сода) NaOH представляет собой белое, гигроскопичное ( притягивающее воду) твердое вещество, легко растворимое в воде. Гидроокись натрия получают или электролизом хлорида натрия ( гл. [34]
Гидроокись натрия является хорошо растворимым в воде относительно легкоплавким веществом. Максимум давления пара эвто-нических растворов систем NaCl - NaOH - ШО и Na2SO4 - - NaOH - НЮ должен быть еще ниже. Если бы не существовали твердые фазы, образованные взаимодействием NaOH с NaCl и N32SO4, то можно было бы утверждать, что полное выпаривание растворов NaOH NaCl Na2SO невозможно осуществить ни при каких температурах, если давление водяного пара превышает только 600 мм рт. ст. Но в результате изучения фазовых равновесий в соответствующих водных и безводных системах было показано, что путем взаимодействия с NaCl и Na2SO4 гидроокись натрия образует несколько твердых фаз. [35]
Гидроокись натрия, калия и аммония хорошо растворимы в воде. Гидроокись кальция, стронция и бария умеренно растворимы. [36]
Гидроокись натрия ( иначе, едкий натр, каустическая сода) потребляется самыми разнообразными отраслями промышленности. [37]
Гидроокись натрия, едкий натр NaOH - белое кристаллическое вещество, расплывающееся на воздухе. [38]
Гидроокись натрия NaOH ( едкий натр) имеет техническое название - каустическая сода. [39]
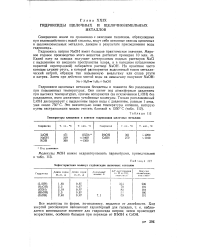 |
Температуры плавления и кипения гидроксидов щелочных металлов. [40] |
Гидроокись натрия NaOH имеет большое практическое значение. Едкий натр на заводах получают электролизом водных растворов Nad с выделением из анодного пространства хлора, а в катодном ( отделенном пористой перегородкой) собирается раствор NaOH. На практике часто катодом служит ртуть, в которой растворяется выделяемый током металлический натрий, образуя так называемую амальгаму или сплав ртути и натрия. [41]
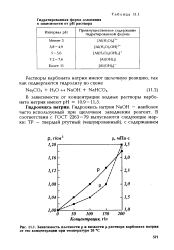 |
Зависимость плотности р и вязкости ц. раствора карбоната натрия от его концентрации при температуре 20 С. [42] |
Гидроокись натрия NaOH - наиболее часто используемый при щелочном заводнении реагент. [43]
Электролитическая гидроокись натрия эффективно очищается от микропримеси железа обработкой 0 05 % - ной амальгамой натрия при 100 С. [44]
Растворяют гидроокись натрия в бидистиллированкой воде. [45]
Страницы: 1 2 3 4