Гидроокись - ванадий
Cтраница 1
Гидроокись ванадия является очень слабым основанием, неустойчивым и легко окисляющимся на воздухе. [1]
Гидроокись ванадия, V ( OH) 3, получают обработкой солей вана-дия ( Ш) щелочью или NH4OH без доступа воздуха. V ( OH) 3 получается в виде зеленого хлопьевидного осадка, легко окисляющегося на воздухе, обладающего слабо основным характером п превращающегося в соли ванадия ( Ш) при растворении в кислотах без доступа воздуха. [2]
Окись и гидроокись ванадия ( П) обладают основным характером и легко растворяются в кислотах с образованием солей. [3]
Химия ванадия очень сложна. Гидроокиси ванадия ( II) и ванадия ( III) обладают основными свойствами, а гидроокиси ванадия в высших состояниях окисления амфотерны. Соединения ванадия окрашены в самые разные цвета. Окись ванадия ( V) V2O5 - вещество оранжевого цвета - применяют в качестве катализатора при контактном методе производства серной кислоты. Метаванадат аммония NH4VO3 образует желтые кристаллы при кристаллизации из раствора. Его применяют для получения препаратов окиси ванадия ( V), используемых в контактном методе производства серной кислоты. [4]
Химия ванадия очень сложна. Гидроокиси ванадия ( П) и ванадия ( 1 II) обладают основными свойствами, а гидроокиси ванадия в высших окислительных состояниях амфотерны. Соединения ванадия окрашены в самые разные цвета. Окись ванадия ( У) V205 - вещество оранжевого цвета - применяют в качестве катализатора при контактном методе производства серной кислоты. Метаванадат аммония NH4V03 образует желтые кристаллы при кристаллизации из раствора. Его применяют при изготовлении препаратов окиси ванадия ( У), используемых в контактном методе производства серной кислоты. [5]
При растворении окиси в разбавленных кислотах образуются соли двухвалентного ванадия. Из этих растворов щелочами осаждают гидроокись ванадия У ( ОН) 2 бурого цвета. Простые соли двухвалентного ванадия, например VS04 - 7H2O, окрашенные в фиолетовый цвет, и комплексные соли, например K4 [ V ( CN) 6 ] - ЗН2О, окрашенные в желтый цвет, изоморфны солям железа. Соединения двухвалентного ванадия очень легко окисляются на воздухе. [6]
В частности, одной из причин повреждения сталей в паре является растворимость в нем ряда легирующих добавок. При высоких давлениях и температурах гидроокиси ванадия, хрома, молибдена и вольфрама заметно растворимы в водяном паре. [7]
Химия ванадия очень сложна. Гидроокиси ванадия ( II) и ванадия ( III) обладают основными свойствами, а гидроокиси ванадия в высших состояниях окисления амфотерны. Соединения ванадия окрашены в самые разные цвета. Окись ванадия ( V) V2O5 - вещество оранжевого цвета - применяют в качестве катализатора при контактном методе производства серной кислоты. Метаванадат аммония NH4VO3 образует желтые кристаллы при кристаллизации из раствора. Его применяют для получения препаратов окиси ванадия ( V), используемых в контактном методе производства серной кислоты. [8]
Химия ванадия очень сложна. Гидроокиси ванадия ( П) и ванадия ( 1 II) обладают основными свойствами, а гидроокиси ванадия в высших окислительных состояниях амфотерны. Соединения ванадия окрашены в самые разные цвета. Окись ванадия ( У) V205 - вещество оранжевого цвета - применяют в качестве катализатора при контактном методе производства серной кислоты. Метаванадат аммония NH4V03 образует желтые кристаллы при кристаллизации из раствора. Его применяют при изготовлении препаратов окиси ванадия ( У), используемых в контактном методе производства серной кислоты. [9]
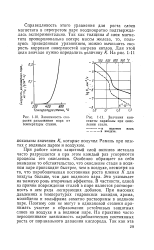 |
Зависимость скорости разложения пара от температуры стенки.| Значения константы параболы при окислении стали. [10] |
При работе котла защитный слой окислов металла часто разрушается и при этом каждый раз ускоряются процессы его окисления. Особенно обращает на себя внимание то обстоятельство, что окисление стали в водяном паре происходит быстрее, чем в воздухе, несмотря на то, что параболическая постоянная роста пленки К, для воздуха больше, чем для водяного пара. Это указывает на важную роль вторичных эффектов. В частности, одной из причин повреждения сталей в паре является растворимость в нем ряда легирующих добавок. При высоких давлениях и температурах гидроокиси ванадия, хрома, молибдена и вольфрама заметно растворимы в водяном паре. Поэтому они не могут в одинаковой степени принимать участие в образовании устойчивых защитных слоев на воздухе и в водяном таре. На практике часто переоценивают зависимость параболических постоянных роста от парциального давления кислорода. [11]
Страницы: 1