Гидроокись - рубидий
Cтраница 2
Гидроокись рубидия, RbOH, образуется при действии воды на металлический рубидий или на его окислы Rb20, Rb202, Rb204; ее получают также взаимодействием баритовой воды Ва ( ОН) 2 с сульфатом или карбонатом рубидия или электролизом раствора карбоната рубидия; при этом используют ртутный катод. Профильтрованный раствор гидроокиси рубидия выпаривают досуха в серебряном сосуде без доступа воздуха и двуокиси углерода. [16]
Растворяют 100 г углекислого рубидия или углекислого цезия в 100 мл дистиллированной воды и к полученному раствору добавляют при непрерывном перемешивании горячий насыщенный раствор гидроокиси бария с небольшим избытком к стехиометрии. Отфильтрованные растворы гидроокисей рубидия или цезия упаривают в серебряных или платиновых чашах при непрерывном кипении с целью уменьшения карбонизации. По мере упаривания небольшой избыток гидроокиси бария, введенный при каустификации, выпадает в осадок, так как IB концентрированных растворах гидроокисей рубидия или цезия гидрат окиси бария нерастворим. [17]
Раствор фильтруют через стеклянный фильтр в колбу. Затем растворяют 6 г гидроокиси рубидия в 16 мл метилового спирта и фильтруют. После охлаждения раствора гидроокиси рубидия до 3 - 5 его прибавляют к осветленному раствору борогидрида натрия, при этом выпадает белый осадок борогидрида рубидия, который отделяется от маточного раствора фильтрацией. Промывной раствор объединяется с маточным раствором и упаривается для выделения большего количества борогидрида рубидия. Общий выход продукта равен 4 5 г, что составляет 90 % от теоретического. [18]
Возможностью получения высших кислородных соединений щелочных металлов интересовались давно. Виллигер [1] заметили, что порошкообразные едкое кали и гидроокись рубидия при взаимодействии с озоном окрашиваются в оранжевый цвет, который при отсутствии влаги сохраняется довольно долго. [19]
Окись рубидия медленно разлагается при нагревании выше 400 на перекись рубидия Rb202 и металлический рубидий. При пропускании тока водорода через нагретую окись рубидия образуется смесь гидрида и гидроокиси рубидия. [20]
Они были получены [46] в виде нечистых препаратов ( с содержанием до 67 % МеО3) действием на гидроокись рубидия и цезия озоном ( или озонированным воздухом)) при - 30 или - 40 и экстрагированием полученных соединений жидким аммиаком при той же температуре с последующим его испарением; основными примесями в МеО3 были гидроокиси рубидия и цезия. [21]
Они были получены [46] в виде нечистых препаратов ( с содержанием до 67 % МеО3) действием на гидроокись рубидия и цезия озоном ( или озонированным воздухом)) при - 30 или - 40 и экстрагированием полученных соединений жидким аммиаком при той же температуре с последующим его испарением; основными примесями в МеО3 были гидроокиси рубидия и цезия. [22]
Раствор фильтруют через стеклянный фильтр в колбу. Затем растворяют 6 г гидроокиси рубидия в 16 мл метилового спирта и фильтруют. После охлаждения раствора гидроокиси рубидия до 3 - 5 его прибавляют к осветленному раствору борогидрида натрия, при этом выпадает белый осадок борогидрида рубидия, который отделяется от маточного раствора фильтрацией. Промывной раствор объединяется с маточным раствором и упаривается для выделения большего количества борогидрида рубидия. Общий выход продукта равен 4 5 г, что составляет 90 % от теоретического. [23]
Растворяют 100 г углекислого рубидия или углекислого цезия в 100 мл дистиллированной воды и к полученному раствору добавляют при непрерывном перемешивании горячий насыщенный раствор гидроокиси бария с небольшим избытком к стехиометрии. Отфильтрованные растворы гидроокисей рубидия или цезия упаривают в серебряных или платиновых чашах при непрерывном кипении с целью уменьшения карбонизации. По мере упаривания небольшой избыток гидроокиси бария, введенный при каустификации, выпадает в осадок, так как IB концентрированных растворах гидроокисей рубидия или цезия гидрат окиси бария нерастворим. [24]
 |
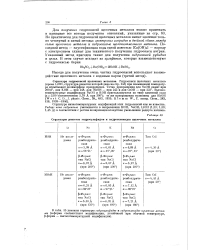
Структуры решеток гидросульфидов и гидроселенидов щелочных металлов. [25] |
Для получения гидроокисей щелочных металлов можно применять в принципе все методы получения оснований, указанные на стр. Но практически для гидроокисей щелочных металлов имеют значение только четвертый и пятый методы: электролиз хлоридов и двойной обмен между солью щелочного металла и гидроокисью щелочноземельного металла. Последний метод - каустификация соды едкой известью [ Са ( ОН) з ] - наряду с электролизом служит для технического получения гидроокиси натрия. Указанный метод пригоден также для получения гидроокисей рубидия и цезия. [26]
 |
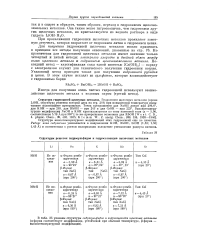
Структуры решеток гидросульфидов и гидроселенидов щелочных металлов. [27] |
Для получения гидроокисей щелочных металлов можно применять в принципе все методы получения оснований, указанные на стр. Но практически для гидроокисей щелочных металлов имеют значение только четвертый и пятый методы: электролиз хлоридов и двойной обмен между солью щелочного металла и гидроокисью щелочноземельного металла. Последний метод - каустификация соды едкой известью [ Са ( ОН) 2 ] - наряду с электролизом служит для технического получения гидроокиси натрия. Указанный метод пригоден также для получения гидроокисей рубидия и цезия. [28]
 |
Структуры решеток гидросульфидов и гидроселенидов щелочных металлов. [29] |
Для получения гидроокисей щелочных металлов можно применять в принципе все методы получения оснований, указанные на стр. Но практически для гидроокисей щелочных металлов имеют значение только четвертый и пятый методы: электролиз хлоридов и двойной обмен между солью щелочного металла и гидроокисью щелочноземельного металла. Последний метод - каустификация соды едкой известью [ Са ( ОН) 21 - наряду с электролизом служит для технического получения гидроокиси натрия. Указанный метод пригоден также для получения гидроокисей рубидия и цезия. [30]
Страницы: 1 2 3