Гидроокись - цинк
Cтраница 1
Гидроокиси цинка, никеля и кобальта ( и частично хрома) растворимы в водных растворах аммиака. [1]
Гидроокись цинка образуется при смешении растворов сернокислого цинка и едкого натра. Полученные осадки соли Шевреля и гидроокиси цинка вводят в ванну с заранее приготовленным раствором цианида и щелочи. Концентрацию свободного цианида корректируют после анализа ванны. Сегнетова соль и аммиак добавляются в последнюю очередь. [2]
Гидроокись цинка весьма мало растворима в воде. Однако некоторое число молекул Zn ( OH) 2 переходит в раствор. Гидроокись цинка является амфотерным соединением. Вследствие этого она образует соли как со щелочами, так и с кислотами. [3]
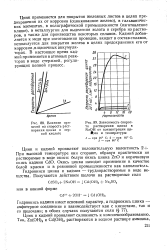 |
Влияние примесей на скорость растворения цинка в серной кислоте.| Зависимость скорости растворения цинка в NaOH от концентрации ще - Лэчи и температуры. [4] |
Гидроокиси цинка и кадмия - труднорастворимые в воде вещества. [5]
Гидроокись цинка подобно гидроокисям других металлов подвержена старению. [6]
Гидроокись цинка является компонентом бинарных систем гидроокисей двухвалентных ( Mg, Co, Ni) [20, 331] и трехвалентных ( А1, Сг, Мп, Fe, Co) [22] металлов, при исследовании которых установлено следующее. [7]
Гидроокись цинка, имеющая значительно большую по сравнению с Fe ( OH) 3 величину произведения растворимости, при действии СаСО3 не осаждается. [8]
Гидроокись цинка растворима и в растворах аммониевых солей. [9]
Гидроокись цинка, Zn ( OH) 2, образуется в виде белого объемистого осадка, если растворы солей цинка обработать щелочами. В кристаллическом состоянии Zn ( OH) 2 существует в виде пяти ( а -, Р -, у -, б -, е -) модификаций, из которых при комнатной температуре только 8 - Zn ( OH) 2 устойчива в воде. Модификация a - Zn ( OH) 2 имеет гексагональную структуру, p - Zn ( OH) 2 - ромбоэдрическую или гексагональную, y - Zn ( OH) 2 - призматическую, 6 - Zn ( OH) 2 - ромбоэдрическую, e - Zn ( OH) 2 - бипирами-дальную структуру. [10]
Гидроокись цинка проявляет амфотерные свойства, растворяется в кислотах, образуя соль и воду, и в щелочах, образуя соль цинковой кислоты H2ZnO2, называемую цинкатом. [11]
Гидроокись цинка подобно гидроокисям других металлов подвержена старению. [12]
Гидроокись цинка является компонентом бинарных систем гидроокисей двухвалентных ( Mg, Co, Ni) [20,331] и трехвалентных ( А1, Cr, Mn, Fe, Co) [22] металлов, при исследовании которых установлено следующее. [13]
Гидроокись цинка Zn ( OH) 2 - аморфный белый порошок. При прокаливании переходит в ZnO. В воде почти не растворяется. [14]
Гидроокись цинка Zn ( OH) 2 - амфотерное соединение, гидроокись кадмия Cd ( OH) 2 обладает основными свойствами со слабо выраженной кислотной функцией, гидраты же окислов Hg ( OH) a и Hg2 ( OH) 2 - неустойчивые соединения. [15]
Страницы: 1 2 3 4