Ацильная гидроперекись
Cтраница 1
Ацильные гидроперекиси - частью жидкости, частью Кристаллические вещества, легко растворяющиеся в органич. Твердые гидроперекиси весьма мало устойчивы. Еще менее стабильны их соли, которые бурно разлагаются под влиянием тепла, выделяющегося при поглощении влаги воздуха. [1]
Ацильные гидроперекиси применяются в органич. [2]
Ацильные гидроперекиси, или органические пер-кислоты, как их иначе называют, получаются действием перекиси водорода на ангидриды кислот или из соответствующих диацильных перекисей и этилата натрия. Они образуются также в качестве промежуточных продуктов при автоокислении альдегидов. [3]
Ацильные гидроперекиси характеризуются резко выраженными окислительными свойствами. Низшие представители быстрее перекиси водорода выделяют иод из йодистого калия. [4]
Ацильные гидроперекиси легко образуют кальциевые соли, свойства которых, однако, мало изучены. Известно, что пермуравышая кислота, вступая в реакцию с карбонатом кальция, дает перформиат кальция. Это соединение очень легко растворяется в воде и спирте. [5]
По мере повышения температуры роль активных продуктов возрастает в следующей последовательности: гидроперекись алкилов - ацильные гидроперекиси - формальдегид. [6]
Из всех реакций оловоорганических соединений с пе-рекисными соединениями наиболее подробно изучено их взаимодействие с ацильными перекисями и ацильными гидроперекисями. [7]
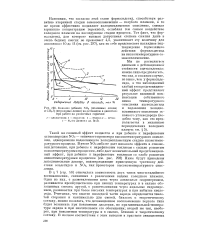 |
Влияние добавок NOa ( сплошные линии. [8] |
Один из них, с разветвлениями цепи через алкильные гидроперекиси, развивается преимущественно при низких температурах и в сильно обогащенных смесях; другой, с разветвлениями через ацильные гидроперекиси, развивается при более высоких температурах и при избытке кислорода. Учитывая, что сжатие последней части заряда определяется теплотой сгорания и максимально для смесей, близких к теоретическому составу, можно полагать, что детонационное воспламенение первого типа будет возникать при повышении давления, но при минимальной температуре заряда и при значительном его обогащении; второй же тип, наоборот, при повышении температуры и в смесях, близких к теоретическому составу. [9]
 |
Зависимость за. [10] |
С изменением степени сжатия может изменяться и относительная роль в холоднопламепном процессе двух механизмов возникновения холодного пламени, которым соответствуют различные оптимальные составы смеси: более бедный - для процесса, идущего через ацильные гидроперекиси, ( см. § 7, стр. [11]
 |
Зависимость задержек холодного T. и голубого Т2 пламен, а также суммарных задержек т. [12] |
С изменением степени сжатия может изменяться и относительная роль в холодноплам: енном процессе двух механизмов возникновения холодного пламени, которым соответствуют различные оптимальные составы смеси: более бедный - для процесса, идущего через ацильные гидроперекиси, ( см. § 7, стр. [13]
Органические перекиси - весьма реакционноспособные и обычно мало устойчивые вещества. Особенно взрывчаты низшие представители алкильных и ацильных гидроперекисей и перекисей, а также алкилиденовые перекиси. [14]
Было найдено, что при употреблении в качестве электролита хлористого лития потенциалы восстановления ацильной гидроперекиси, гидроперекисей, оксиперекисей, перекисей алкилов и перекиси водорода не совпадают друг с другом и равны - 0 1; - 0 25; - 0 4 - 0 55 и - 0 8 в, соответственно. [15]
Страницы: 1 2