Гидросульфат - натрий
Cтраница 1
Гидросульфат натрия технический Na2S2O4 ( ГОСТ 246 - 67) - безводная натриевая соль гидросернистой кислоты. Порошок белого цвета выпускается 1-го и 2-го сортов в зависимости от содержания основного вещества ( 90 и 85 %) и допускаемых примесей. Хранят в сухих помещениях, в металлических герметичных барабанах. Самопроизвольно разогревается от попадания влаги и воздуха. [1]
Гидросульфат натрия технический Na2S2O4 ( ГОСТ 246 - 76) - безводная натриевая соль гидросернистой кислоты. [2]
Гидросульфат натрия технический Na2S204 ( ГОСТ 246 - 76) - безводная нат-риевая соль гидросернистой кислоты. [3]
Гидросульфат натрия и пиросульфат натрия применяют в химическом анализе для вскрытия труднорастворимых соединений. Их используют также для очистки платиновых тиглей. [4]
Гидросульфат натрия технический Na Ss04 ( ГОСТ 246 - 41) - безводная натриевая соль гидросернистой кислоты. Выпускается 1 и 2-го сортов в зависимости от содержания основного вещества и допускаемых примесей. [5]
Гидросульфат натрия ведет себя аналогично, хотя чистый Na2SjO7 получается с трудом. [6]
Гидросульфат натрия и пиросульфат натрия применяют в химическом анализе для вскрытия труднорастворимых соединений. Их используют также для очистк платиновых тиглей. [7]
Раствор гидросульфата натрия должен быть приготовлен в тех же условиях, в которых сплавляют навеску тантала с гидросульфатом натрия. Для этого в кварцевые стаканчики отвешивают по 4 г безводной соли и нагревают в муфеле почти до прекращения выделения паров серной кислоты. Содержимое растворяют в воде из расчета получения 8 % - ного раствора. [8]
В воде гидросульфат натрия диссоциирует на ион натрия, ион водорода и сульфат-ион. Ион водорода придает раствору кислый характер; например, такой раствор может вызывать покраснение синей лакмусовой бумаги. [9]
ЬО ( гидросульфата натрия) для тушения флюоресценции рибофлавина и снова делают отсчеты флюоресценции примесей. [10]
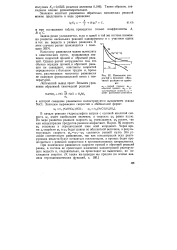 |
Изменение ско. [11] |
В начале реакции гидросульфата натрия с соляной кислотой скорость W-L имеет наибольшее значение, а скорость ш2 равна нулю. По мере развития реакции скорость шх уменьшается, w2 растет, так как концентрации продуктов реакции возрастают. На рис. 92 скорость w2 отложена в отрицательной зоне осей координат. Через время ( 0 скорости Wi и w2 будут равны по абсолютной величине, а результирующая скорость шрпуг-ш 2 сделается равной нулю. Это условие соответствует равновесию, так как концентрации всех реагирующих веществ будут оставаться постоянными, а процесс будет продолжаться с равными скоростями в противоположных направлениях. [12]
 |
Изменение скоростей. [13] |
В начале реакции гидросульфата натрия с соляной кислотой скорость Wi имеет наибольшее значение, а скорость да 2 равна нулю. По мере развития реакции скорость w уменьшается, ш2 растет, так как концентрации продуктов реакции возрастают. На рис. 84 скорость w2 отложена в отрицательной зоне осей координат. [14]
 |
Изменение скоростей в процессе обратимой реакции во времени. [15] |
Страницы: 1 2 3 4