Гидрофильность - поверхность
Cтраница 1
Гидрофильность поверхности всех трех образцов проявлялась в их значительной влагоемкости. Предположение, что гидрофильность бора связана с частичной окисленностью поверхности его частиц, было подтверждено экспериментально. [1]
Гидрофильность поверхности двуокиси кремния определяется его структурными свойствами. В идеальном случае поверхность SiO2 состоит из силоксановых мостиков. [2]
Таким образом, гидрофобность или гидрофильность поверхности поверхностно-активных веществ зависит от полярной фазы, на границе с которой образовалась или находится эта поверхность. Это дает возможность получать гидрофобные или гидрофильные поверхности. Для того, чтобы полученная та или иная поверхность в дальнейшем не изменяла свою смачиваемость, следует предотвратить возможность переориентации поверхностных молекул, для чего необходима их химическая фиксация. [3]
 |
Изменения в точении опыта относительной скорости электроосмотического вытеснения при / - 0 3 ма. [4] |
Предположение о существенном влиянии степени гидрофильности поверхности на характер кривых скорость электроосмотического вытеснения - время, очевидно, могло быть проверено на системах, имеющих ту же структуру норового пространства, но иные углы смачивания. Однако применение ПАВ могло накладывать свое влияние на характер кривых не только вследствие гидрофобизации поверхности, но и вследствие других свойств образующихся адсорбционных слоев - степени их развития и прочности. Для того чтобы избежать этих дополнительных влияний, далее сопоставляются результаты, полученные только на тех системах, где образующиеся адсорбционные слои либо не разрушались, либо, если и разрушались, то в весьма малой степени. Как указано в работе [1], о степени разрушения их в тех или иных условиях мы считаем возможным судить косвенно по изменению процента вытеснения в зависимости от величины применяемой силы тока. [5]
Затем приступают к исследованию изменения гидрофильности поверхности образцов в результате озонирования и прививки по углу смачивания. Для этого образцы 1, 2 и 3 последовательно помещают на предметное стекло, прижимают скобками и наносят на каждый из них каплю дистиллированной воды. [6]
Кроме того, при изменении степени гидрофильности поверхности сравнительно высокодисперсных суспензий ( исходные частицы которых имеют размеры порядка 0 1 - 10 мк) часто происходит изменение структуры осадка. [7]
Отсюда следует, что для резкого повышения гидрофильности поверхности достаточно присутствия на ней групп СООН или СН5ОН в незначительной пропорции. [8]
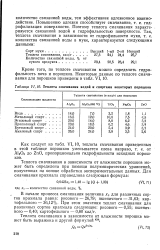 |
Теплота смачивания водой и спиртами некоторых порошков. [9] |
Поэтому теплота смачивания характеризуется связанной водой и гидрофильностью поверхности. [10]
Следует отметить, что указанные процессы включают в себя эффект понижения гидрофильности поверхности глинистых минералов, что в ряде случаев превалирует над увеличением их дисперсности за счет расклинивающего давления при действии ПАВ. Необходимо также учитывать при этом частичную термическую деструкцию его молекул, усиливающую противоположно направленный эффект агрегирования частиц дисперсной фазы. [11]
Сущность этих явлений обусловлена как возникновением электрических зарядов, так и гидрофильностью поверхности глинистых частиц. Шарову [36] электрические заряды возникают в результате поверхностного растворения глинистых частиц и диссоциации гидратирующих катионов. При этом наиболее активными частями поверхности будут места изломов кристаллической решетки, углы и ребра частиц. Однако согласно П. А. Ребиндеру [29] углы и ребра частиц являются наименее гидрофильными, что и вызывает взаимное притяжение частиц. Это противоречие объясняется наиболее высокой интенсивностью реакций обмена в активных частях решетки с заменой в обменном комплексе гидрофильных ионов натрия на ионы кальция, обусловливающими гидрофобизацию поверхности по мере вытеснения. [12]
При адсорбции ионов и создании двойного электрического слоя на поверхности коллоидных частиц гидрофильность поверхности возрастает в результате собственной гидратации ионов и влияния зарядов поверхности на ориентированную адсорбцию дипольных молекул воды; так, например, возрастает смачивание заряженной поверхности ртути. Однако в этом случае гидратные слои полностью зависят от ионных взаимодействий и при наступлении коагуляции коллоидов электролитами не препятствуют процессу слипания частиц. Поэтому в типично лиофобных золях ( Аи, Ag, S, As2S3 и др.) сразу после перехода порога коагуляции наблюдается помутнение раствора, изменение цвета, выпадение осадка и другие проявления коагуляции. [13]
При адсорбции ионов и создании двойного электрического слоя на поверхности коллоидных частиц гидрофильность поверхности возрастает в результате собственной гидратации ионов и влияния зарядов поверхности на ориентированную адсорбцию дипольных молекул воды. Так, например, возрастает смачивание заряженной поверхности ртути. В этом случае гидратные слои полностью зависят от ионных взаимодействий и при наступлении коагуляции коллоидов электролитами не препятствуют процессам слипания частиц. Если же поверхность коллоидных частиц сама является гидрофильной или способна к образованию молекулярных соль-ватных слоев, коллоидные частицы могут сохраниться в состоянии золя даже при переходе порога коагуляции. Так, например, высокоочищенные золи кремнекислоты или А1203 могут сохраниться в растворе даже при падении электрофоретической подвижности ( - потенциала) почти до нуля. [14]
Как известно, степень заполнения подложки ОН-группами проявляется в той или иной степени гидрофильности поверхности образца. [15]
Страницы: 1 2 3 4