Электрофильная активность
Cтраница 1
Электрофильная активность этих веществ, однако, относительно невелика и должна быть повышена действием кислот Льюиса или протонных кислот. При этом кислотный катализатор [ Е в схеме ( 198) ] атакует атом кислорода карбонильного соединения или атом азота карбониланалогичного соединения и, оттягивая электроны, повышает положительный заряд соседнего атома углерода. [1]
Электрофильная активность XNO в реакциях нитрозирования зависит от природы X. Для них рассчитаны общие энергии, длины связей, углы между связями. [2]
По электрофильной активности диазотирующие агенты располагаются в ряд: ON ON - OH2 ON - C1 ON - Br ON - NO2 ON - ОН. [3]
Ввиду слабой электрофильной активности двуокиси углерода терефталевая кислота образуется лишь при высокой температуре. [4]
Льюиса, повышает электрофильную активность карбонильной группы. Одновременно негативированный, комплексно связанный атом алюминия вызывает сдвиг электронов в исходящих от него связях. [5]
 |
Реакции карбонильных соединений с криптооснованиями. [6] |
Льюиса, повышает электрофильную активность карбонильной группы. Одновременно комплексно связанный негативированный атом алюминия вызывает сдвиг электронов в исходящих от него связях. [7]
Заметим, что и электрофильная активность присуща только образцам иммобилизованных катализаторов, приготовленных в присутствии ароматических соединений. По-видимому, кроме активации связанной комплексной кислоты, присутствие ароматического растворителя обеспечивает сольватирующую ( растворяющую) способность в отношении образующегося на поверхности катализатора полимера, в частности полиизобутилена. При сополимеризации винилсили-лового эфира с изобутиленом, несмотря на заметно меньшую активность последнего, происходит, очевидно, ослабление хемосорбции полярного полимера на полярной поверхности иммобилизованного катализатора и образование со полимерного продукта. Так как индивидуально взятые компоненты - сульфокатионит и алюми-нийхлорид - вызывали только раздельную полимеризацию указанных иономеров, иммобилизованная комплексная система сближает соотношение их активностей. [8]
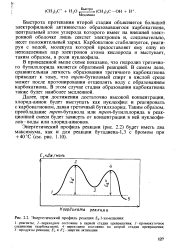 |
Энергетический профиль реакции SN 1-замещения. [9] |
Быстрота протекания второй стадии объясняется большой электрофильной активностью образовавшегося карбокатиона, центральный атом углерода которого имеет на внешней электронной оболочке лишь секстет электронов и, следовательно, несет положительный заряд. Карбокатион стабилизуется, реагируя с водой, молекула которой предоставляет ему одну из неподеленных пар электронов атома кислорода и выступает, таким образом, в роли нуклеофила. [10]
Эта мезомерия является одной из причин электрофильной активности изоцианатов. Последняя основывается как на различиях в степени электроотрицательности атомов азота, углерода и кислорода в системе куму лир ованных двойных связей, так и на том факте, что присоединению нуклеофильного компонента реакции соответствует изменение гибридизации С-атома изоцианата. [11]
Напротив, в молекуле а-изатинхлорида ( 68) электрофильная активность выше у сс-углеродного атома, положительный заряд на котором увеличивается сильным индукционным влиянием атома хлора, тогда как на 3-углеродном атоме он снижается сопряжением с атомом азота. [12]
Образование именно 1-хлор, а не 3-хлорпроизводного объясняется более высокой электрофильной активностью положения 1 по сравнению с положением 3 ( стр. [13]
Из приведенных формул очевидно, что в случае введения группы N02 электрофильная активность иона диазония увеличивается ввиду усиления электронного дефицита у диазогруппы. Группа ОСН3, наоборот, снижает электронный дефицит у диазогруппы и тем самым дезактивирует ее. [14]
Из приведенных формул видно, что в случае введения группы NO2 электрофильная активность иона диазония увеличивается ввиду усиления электронного дефицита у диазогруппы. Группа ОСН3, наоборот, снижает электронный дефицит у диазогруппы и тем самым дезактивирует ее. [15]
Страницы: 1 2 3