Гипофосфит
Cтраница 2
Гипофосфит лития LiH2PO2 весьма гигроскопичен, хорошо растворяется в воде, выделяется в виде LiH2PO2 - H2O, при нагревании разлагается с воспламенением. [16]
Гипофосфит целлюлозы, содержащий 4 5 % фосфора, негорюч; однако недостаточная стойкость к действию гидролизующих реагентов, в частности кипящей воды, затрудняет возможность практического использования этих производных целлюлозы. [17]
Гипофосфит Ge ( H2PO2) 4 был получен в результате двухчасового выдерживания при 100 С ( при постоянном перемешивании) смеси GeI2 с 90 % - ной Н3РО2 в контакте с воздухом для окисления двухвалентного германия до четырехвалентного. [18]
Гипофосфит бария легко очищается перекристаллизацией. [19]
Гипофосфит бария легко очищается перекристаллизацией. В сильнокислой среде ( особенно при нагревании) она является очень энергичным восстановителем. Напротив, в разбавленных растворах на холоду Н3Р02 не окисляется ни кислородом воздуха, ни свободным иодом. [20]
Кислый гипофосфит Th ( Н2РО3) 4, легко растворяющийся в конц. [21]
Гипофосфит лития LiHoPOo получается по реакции между Ва ( Н2РО2) 2 и LiOH в водном растворе; из раствора выделяется моногидрат в виде мелких бесцветных гигроскопичных кристаллов моноклинной сингонии. [22]
Все гипофосфиты растворимы в воде. [23]
Если исходный гипофосфит легко гидролизуется до глюкозы и фосфорноватистой кислоты, то продукт изомеризации не изменяется при длительном нагревании с кислотами и щелочами. [24]
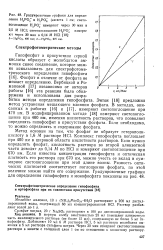 |
Градуировочные графики для определения Н2РО2 - и Н2РО4 ( кювета 1 светопоглощение H2POJ измеряют через 30 мин в 2 5 М НС1. светопоглощение Н2РО - измеряют через 30 мин в 0 14 М НС1. [25] |
Комплекс гипофосфита поглощает при 400 нм в широкой области кислотности растворов. Если нужно определять фосфат, кислотность раствора во второй аликвотной части доводят до 0 14 М по НС1 и измеряют светопоглощение при 670 нм. Если известна концентрация гипофосфита и оптическая плотность его раствора при 670 нм, можно учесть ее вклад в суммарное светопоглощение при этой длине волны. Разность оптических плотностей соответствует поглощению фосфата, по этой величине можно найти его содержание. [26]
Изомеризацией гипофосфитов мы синтезировали несколько фосфонистых кислот в ряду пентоз и гексоз, что позволяет начать широкое изучение этих интересных фосфорсодержащих производных Сахаров. [27]
Расход гипофосфита составляет 5 г на 1 г выделившегося металлического никеля. [28]
Расход гипофосфита на образование покрытия изменяется в зависимости от условий проведения реакции. Наибольший коэффициент использования гипофосфита не превышает 40 % от общего его количества, содержащегося в растворе. [29]
Навеску гипофосфита 1 г, взвешенную с точностью до 0 001 г, растворяют в кварцевой чашке в 5 мл воды. К раствору прибавляют 4 мл азотной кислоты и 2 капли перекиси водорода для удаления органических веществ и выпаривают на водяной бане досуха. После охлаждения к остатку добавляют 5 мл воды и 2 мл азотной кислоты и вновь выпаривают досуха. [30]
Страницы: 1 2 3 4