Химическая активность - металл
Cтраница 1
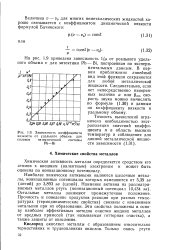 |
Зависимость коэффициента. [1] |
Химическая активность металла определяется сродством его атомов внешним ( валентным) электронам и может быть оценена по ионизационному потенциалу. [2]
Химическая активность металлов этой группы от Zn к Hg уменьшается. [3]
Химическая активность металлов различна. Такие металлы, как натрий Na, калий К, кальций Са, обладают очень высокой химической активностью, вступая в реакции с неметаллами, водой, кислотами при комнатных условиях. Есть металлы, которые называются благородными ( золото Аи, платина Pt) из-за их очень слабой химической активности. Благородные металлы с большим трудом реагируют даже с очень сильными окислителями. [4]
Химическая активность металлов в подгруппе хрома уменьшается от хрома к вольфраму. [5]
Химическая активность металлов уменьшается с увеличением количества электронов во внешнем электронном слое. Поэтому в реакциях, протекающих в отсутствие воды, кальций менее активен, чем натрий. [6]
Химическая активность металла определяется, как известно, сродством его атомов к внешним ( валентным) электронам и может быть оценена по величине ионизационного потенциала. [7]
 |
Некоторые свойства Си, Ag, Аи. [8] |
Химическая активность металлов Си, Ag, Аи сравнительно невелика. С кислородом реагирует только медь, благородные металлы Ag и Аи не окисляются кислородом даже при нагревании. При комнатной температур-е Си практически не взаимодействует с фтором вследствие образования прочной защитной пленки фторида. Хлориды СиСЬ, AgCl, АиС13 также образуются в результате взаимодействия элементных веществ при нагревании. [9]
 |
Некоторые свойства Си, Ag, Аи. [10] |
Химическая активность металлов Си, Ag, Аи сравнительно невелика. С кислородом реагирует только медь, благородные ме-рллы Ag и Аи не окисляются кислородом даже при нагревании. При комнатной температуре Си практически не взаимодействует с фтором вследствие образования прочной защитной пленки фторида. При нагревании Си и Ag реагируют с серой, образуя Cu2S и AgaS. Хлориды СиСЬ, AgCl, АиС13 также образуются в результате взаимодействия элементных веществ при нагревании. [11]
 |
Некоторые свойства меди, серебра и золота. [12] |
Химическая активность металлов Си, Ag, Аи сравнительно невелика. С кислородом реагирует только медь, благородные металлы Ag и Аи не окисляются кислородом даже при нагревании. При комнатной температуре медь практически не взаимодействует со фтором вследствие образования прочной защитной пленки фторида. Хлориды CuCl2, AgCl, AuCb также образуются в результате взаимодействия элементных веществ при нагревании. [13]
 |
Некоторые свойства меди, серебра и золота. [14] |
Химическая активность металлов Си, Ag, Аи сравнительно невелика. С кислородом реагирует только медь, благородные металлы Ag и Аи не окисляются кислородом даже при нагревании. При комнатной температуре медь практически не взаимодействует со фторсм вследствие образования прочной защитной пленки фторида. При нагревании Си и Ag реагируют с серой, образуя сульфиды CujS и AgjS. Хлориды CuClj, AgCl, AuCh также образуются в результате взаимодействия элементных веществ при нагревании. [15]
Страницы: 1 2 3 4