Гитторф
Cтраница 1
Гитторф [1] при определении чисел переноса ионон пытался использовать некоторые диафрагмы для уменьшения диффузии электролита из анодного пространства в катодное. Он нашел, что применение животных диафрагм отклоняло значения получаемых чисел переноса от тех, которые получаются без применения диафрагм. Еще раньше Рейсом [2] было замечено движение жидкости через диафрагмы при пропускании тока через систему жидкость - диафрагма. [1]
Гитторф, экспериментируя с разрядной трубкой, пришел к выводу, что от катода прямолинейно распространяются неизвестные лучи. [2]
Гитторф показал, что при электролизе движение катиона и аниона происходит в противоположных направлениях с различной скоростью, что зависит от их природы. [3]
 |
Схема движения ионов и изменения концентраций в приэлектродных слоях. [4] |
Гитторф в 1853 г. обнаружил, что при прохождении тока в слоях электролита, прилегающих к катоду ( като-лите) и к аноду ( анолите), изменяются концентрации растворенного вещества. Эти изменения были объяснены различием в скоростях движения ионов. [5]
Гитторф и Сальковский [14], Диттенбергер и Диц [15] определяли числа переноса для растпоров хлорной платины. [6]
Гитторф и Сальковский еще в 1899 г. показали, что АиС13 с водой образует комплексную кислоту Н2 [ АиС13О ]; с соляной кислотой АиС13 дает комплексную кислоту и только при наличии избытка в электролите ионов хлора против формулы золотохлорводородной кислоты НАиС14 золото на аноде растворяется с образованием аниона АиСГГ - Чем выше анодная плртность тока, тем больше должна быть концентрация избыточного хлористого водорода или хлористого натрия в электролите. [7]
Гитторф, изучавший движение ионов при электролизе, доказал, а позднейшие экспериментальные данные подтвердили, что противоположно заряженные ионы перемещаются с разными скоростями. [8]
Гитторфа и истинное число переноса делаются почти равными. Изменение чис а переноса Гитгорфа с разбавлением может таким образом явиться не только следствием образования комплексов, но также и гидратации. [9]
Гитторфа, в котором числа переноса определяют по изменению концентрации раствора в при-электродном отсеке. [10]
Гитторфа, не отвечают их истинным значениям. Разные сорта ионов движутся с различными скоростями и связаны не с одним и тем же числом молекул воды, поэтому изменение концентрации вблизи электрода будет следствием уменьшения ( или увеличения) не только числа частиц растворенного вещества, но и числа молекулы воды. [11]
Гитторфа, не отвечают их истинным значениям. Разные сорта ионов движутся с различными скоростями и связаны не с одним и тем же числом молекул воды, поэтому изменение концентрации вблизи электрода будет следствием уменьшения ( или увеличения) не только числа частиц растворенного вещества, но и числа молекул воды. [12]
Далее Гитторф установил, что отношение UIV не зависит от разности потенциалов на электродах; влияние температуры в определенных пределах оказывается незначительным. Анализируя и обобщая данные своих опытов, Гитторф высказал ряд ценных положений, значение которых было понято в полной мере только после создания теории электролитической диссоциации. Интересны его высказывания о том, что появление ионов не должно являться результатом действия электрического тока, что ионы электролита не могут быть связаны твердым образом в молекулах. [13]
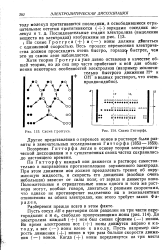 |
Схема Гротгуса.| Схема Гитторфа. [14] |
По Гитторфу каждый ион движется в растворе самостоятельно в направлении противоположно заряженного электрода. При этом движении ион должен преодолевать трение об окружающую жидкость, и скорость его движения ( вообще очень небольшая) зависит от силы поля; от заряда и диаметра иона. Положительные и отрицательные ионы одного и того же раствора могут, вообще говоря, двигаться с разными скоростями, что однако не противоречит выделению их в эквивалентных отношениях на обоих электродах, как этого требует закон Фа - р адея. [15]
Страницы: 1 2 3 4