Гликозилтрансфераза
Cтраница 1
Гликозилтрансферазы играют важную роль в синтезе гликозаминогликанов и гликопротеидов. Перечень гликозилтрансфераз, нуждающихся в марганце в качестве кофактора, весьма обширен. К числу этих ферментов относятся галактозил - и N-ацетилгалактозаминилтрансферазы и ксилозилтрансфераза, осуществляющая перенос ксилозы на белковую часть гликопротеидов. При дефиците марганца нарушено также включение сульфата в хрящевую ткань. [1]
Гликозилтрансферазы существуют, вероятно, в форме полиферментных комплексов, и это, видимо, один из тех редких примеров в природе, когда специфическая последовательность олиго-мерной молекулы синтезируется из ряда строительных блоков ( в отличие от синтеза белков) безучастия матрицы. [3]
Гликозилтрансферазы - ферменты, ускоряющие реакции переноса гликозидных остатков из молекул фосфорных соединений к молекулам моносахаридов, полисахаридов в др. В этой группе выделяют гекеозилтрансферазы, переносящие остатки гексоз, и п е в т о з ил трансферазы, переносящие остатки пентоз. [4]
Способность сахарозофосфорилазы действовать в качестве гликозилтрансферазы указывает на возможность участия аналогичных ферментов в синтезе и расщеплении олигосахаридов. [5]
Другое открытие А. Н. Петровой сводится к установлению ранее неизвестных свойств обнаруженного ею фермента декстрин-4 - гликозилтрансферазы, сокращенно ДГТ. Декстрины - это сахара, на которые действует фермент. Цифра 4 указывает на характер связи между частицами углевода, образующейся при действии фермента. Слово трансфераза характеризует действие фермента - перенос сахара от одного углевода к Другому. ДГТ играет важную роль в углеводном обмене. С одной стороны, в зависимости от потребности организма он может превращать сложные углеводы в простые. С другой стороны, этот фермент обладает способностью строить сложный полисахарид из простых Сахаров, запасая таким образом энергию в печени в виде гликогена. Последующее изучение свойств и особенностей фермента и механизма его действия привело автора открытия к важному выводу: ДГТ может находиться в организме в очень активной и в малоактивной формах. На основе этого ведется поиск путей управления его действием. [6]
Гликозилтрансферазы играют важную роль в синтезе гликозаминогликанов и гликопротеидов. Перечень гликозилтрансфераз, нуждающихся в марганце в качестве кофактора, весьма обширен. К числу этих ферментов относятся галактозил - и N-ацетилгалактозаминилтрансферазы и ксилозилтрансфераза, осуществляющая перенос ксилозы на белковую часть гликопротеидов. При дефиците марганца нарушено также включение сульфата в хрящевую ткань. [7]
Перенос гликозильного остатка легко осуществляется ферментами данной группы, когда субстратом служат нуклеозиддифосфомоносахарид, особенно УДФглюкоза. Нуклеозиддифосфосахара являются коферментами гликозилтрансфераз. Например, биосинтез сахарозы в растительных тканях осуществляется ферментом УДФглюкоза: D-фруктоза - 2 глюкозилтрансфераза ( К. [8]
Реакции переноса гликозильных групп от нефосфорилированных углеводов осуществляются не только истинными, способными только к данной реакции ферментами [34], но и большим числом гидролитических ферментов - карбогидраз. Последние ведут себя в зависимости от условий и как гидролазы, и как гликозилтрансферазы. [9]
 |
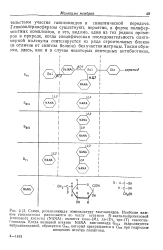
Перенос UDP-активированного сахара на сериновую гидроксильную.| Полипренол долихол - промежуточный липнд, участвующий в биосинтезе N-гликозндной связи гликопротеинов. [10] |
Каждая молекула гликопротеина может включать несколько идентичных олигосахаридных цепей, которые специфичны для данного белка. Однако последовательности олигосахаридов необязательно должны быть полными: один или более моносахаридов могут отсутствовать. Структура олигосахаридов определяется специфическими гликозилтрансферазами. [11]
При длительном хранении сырья в нем начинают преобладать процессы распада. Особенно сложен обмен углеводов в клубнях картофеля. Синтез и гидролиз крахмала в них осуществляются не амилазами, а фосфорилазами ( гликозилтрансферазами), обладающими способностью переносить гликозил ( остаток моносахарида, не содержащего гликозидного кислорода) на фосфорную кислоту с образованием глюкозо-1 - фосфата. [12]
Гликопротеины содержат олигосахаридные цепи, структуры которых придают исключительное специфичное разнообразие поверхностям мембран. Эти цепи связаны с остатками серина или треонина через О-гликозидные связи или с аспарагиновыми остатками через N-гликозидные связи. Связывание осуществляется непосредственно через UDP-caxapa или в случае N-глико-зидов через промежуточные долихоловые производные с участием специфических гликозилтрансфераз. Функции олигосаха-ридных цепей гликопротеинов в адгезии клеток и узнавани еще предстоит выяснить. [13]
Страницы: 1