Глутаматдегидрогеназа
Cтраница 1
Глутаматдегидрогеназа локализуется главным образом или исключительно в митохондриях клеток высших растений. Однако этот фермент легко освобождается из изолированных митохондрий и может быть полностью переведен в раствор путем обработки детергентами. Локализация фермента в митохондриях свидетельствует о том, что Глутаматдегидрогеназа тесно связана с ферментами, катализирующими реакции цикла трикарбоновых кислот, ответственные за образование как а-кетоглутарата, так и восстановленных пиридиннуклеотидных кофер-ментов. Поэтому в митохондриях создаются благоприятные условия для прямой реакции2, ведущей к синтезу глутаминовой кислоты. [1]
Глутаматдегидрогеназа является одним из наиболее изученных ферментов белкового обмена. Он выполняет важную регуляторную функцию не только в аминокислотном, но и энергетическом обмене. [2]
Именно глутаматдегидрогеназа от - остатков. [3]
Для кристаллической глутаматдегидрогеназы из печени характерна высокая субстратная специфичность, однако она осуществляет аминиро-вание а-кетовалериановой кислоты с образованием L-норвалина - аминокислоты, до сих пор не обнаруженной у высших организмов. [4]
Согласно существующим представлениям, реакция, катализируемая глутаматдегидрогеназой ( рис. 14 - 2, стадия а; см. также гл. Роль восстановителя в этой реакции может играть либо NADH, либо NADPH. В эукариотических клетках глутамат-дегидрогеназа находится преимущественно в митохондриях. Далее под действием трансаминаз внутри и вне митохондрий азот глутаминовой кислоты перераспределяется, включаясь в другие аминокислоты. Особенно активна аспартатаминотрансфераза ( гл. [5]
 |
Ингибирование глутаматдегидрогеназы по принципу обратной связи под действием НАД Н и высокого энергетического заряда. [6] |
Все рассмотренные выше регуляторные свойства реакции, катализируемой глутаматдегидрогеназой, указывают на существенную роль этого фермента в энергетическом обмене. [7]
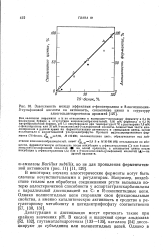 |
Зависимость между эффектами о-фенантролина и 8-оксихинолин. [8] |
В кислой и щелочной среде альдолаза [52, 132], глутаматдегидрогеназа [133-135], каталаза [54] диссоциируют до субъединиц или полипептидных цепей. [9]
Интересно отметить, что, как показало изучение кристаллической глутаматдегидрогеназы из печени, этот фермент катализирует ряд обратимых реакций окислительного дезаминиро-вания аминокислот, включая реакцию окислительного дезамини-рования L-аланина. Глутаматдегидрогеназа состоит из четырех субъединиц, которые при совместном действии катализируют реакцию с глутаминовой кислотой. По отдельности же эти субъединицы активны по отношению к аланину, а не глутаминовой кислоте. [10]
Эйлером открыт высокоактивный при физиологических значениях рН специфический фермент ( глутаматдегидрогеназа), катализирующий окислительное дезаминирование L-глутаминовой кислоты. Он является анаэробным ферментом и чрезвычайно широко распространен во всех живых объектах. [11]
 |
Стандартные окислительно-восстановительные потенциалы Е некоторых биологических систем. [12] |
Матрикс содержит ферменты цикла трикарбоновых кислот, р-окисления жирных кислот, синтеза мочевины, аспартатаминотрансферазу, глутаматде-гидрогеназу, фосфоенолпируваткарбоксикиназу и др. Определение активности глутаматдегидрогеназы и малатдегидрогеназы часто используют для идентификации матрикса митохондрий. [13]
 |
Влияние аденина ( А, добавленного к тимоцитам после облучения, на жизнеспособность клеток и содержание в них АТФ [ Ohyama H., Yama - da Т., 1970 ]. [14] |
Вместе с тем в ядерной оболочке тимоцитов обнаружены цитохромы, соответствующие дыхательной цепи митохондрий, и окислительные ферменты: цитохромоксидаза, NADH2 - и NADHPHg-цитохром-с - редуктаза, глутаматдегидрогеназа. Ядра тимоцитов способны к синтезу АТФ в аэробных условиях, причем этот процесс зависит от ДНК. Следует отметить, что окислительное фосфорили-рование происходит не только в ядрах тимоцитов и лимфоидных тканей, но и в ядерных мембранах печени. [15]
Страницы: 1 2 3