Диффузия - ион - медь
Cтраница 2
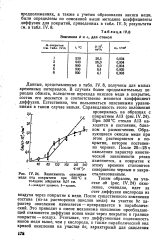 |
Зависимость окисления меди под покрытием при 500 С и. [16] |
После существенного изменения состава ( из-за растворения окислов меди) на участке be характер окисления изменяется - превращается в параболический. Это приводит к смене механизма окисления: преобладающей становится диффузия ионов меди через покрытие к границе покрытие - воздух. [17]
Согласно механизму окисления, предложенному Вагнером, окислы образуются на поверхности соприкосновения меди и кислорода. При этом рост толщины пленки окисла осуществляется за счет диффузии ионов меди из металла через слой окисла. По этому механизму, вначале окисная пленка образуется за счет радиоактивной меди, присутствовавшей на поверхности. Именно такое выворачивание и было наблюдено экспериментально. [18]
Окислы, несомненно, начинают образовываться на поверхности металла. Дальнейший рост толщины их пленки, по теории Вагнера, происходит в результате диффузии ионов меди к поверхности через слой окисла. [19]
Избыток сульфата никеля ( последний как примесь чаще всего встречается в аноде) затрудняет процесс рафинирования. Участвуя в переносе тока, ионы никеля скапливаются в прика-тодном слое, затрудняя диффузию ионов меди. Катодные осадки становятся рыхлыми, кристаллы не связанными ( см. рис. 61 - 62), появляются в-ключения раствора, на катоде начинается разряд ионов примесей, потенциалы которых близки к потенциалу меди. [20]
При перемешивании электролита сжатым воздухом плотность тока может быть увеличена до ( 5 - 30) 102 А / м2 в зависимости от интенсивности перемешивания, температуры электролита, размеров и формы покрываемых изделий. Несмотря на высокую кислотность электролита выделение водорода на катоде не происходит вплоть до предельного тока диффузии ионов меди. Это объясняется тем, чтсЛгри данных условиях потенциалы выделения меди имеют более положительные значения, чем потенциалы выделения водорода. [21]
Концентрация сернокислой меди в ванне может быть тем выше, чем выше температура электролита и чем интенсивнее перемешивание раствора. Повышение температуры сернокислого электролита приводит к снижению и без того малой катодной поляризации и к образованию более грубого покрытия. Однако, если процесс осаждения совершается при высокой катодной плотности тока, то повышение температуры необходимо, чтобы повысить скорость диффузии ионов меди из глубины электролита в прикатодный слой. С этой же целью вводится перемешивание раствора. [22]
Концентрация медного купороса в ванне может быть тем выше, чем выше температура электролита и чем интенсивнее перемешивание раствора. Повышение температуры сернокислого электролита приводит к снижению и без того малой катодной поляризации и к образованию более грубого покрытия. Однако, если процесс электролиза совершается при 1высокой катодной плотности тока, то повышение температуры электролита необходимо, чтобы повысить скорость диффузии ионов меди из глубины электролита в катодный слой. С этой же целью вводится пере-смешивание раствора. [23]
Эта реакция идет на границе раздела фаз: электролит - зерно никелевого порошка. При взаимодействии поверхность зерна никеля покрывается пленкой цементной меди. Ионы диффундируют к поверхности никеля через ламинарный подслой электролита и через поверхностную пленку цементной меди. В результате скорость процесса цементации складывается из скорости реакции на поверхности взаимодействия и скорости диффузии ионов меди к поверхности никеля. Кинетика этого процесса во многом аналогична кинетике процесса обжига гранулированной шихты в кипящем слое. [24]
Следует отметить, что число переноса t в равенстве ( 5 - 3) применяется в области неоднородной концентрации. Оно по-прежнему является фундаментальным свойством транспорта, связанным с подвижностью соотношением ( 5 - 4), однако больше не определяет долю тока, переносимую каким-либо ионным компонентом. Коэффициент D оказывается коэффициентом диффузии сульфата меди, определяющим скорость, с которой сульфат меди диффундировал бы в отсутствие тока. Он имеет промежуточное значение между коэффициентами диффузии ионов меди и сульфата. [25]
Следует отметить, что число переноса t в равенстве ( 5 - 3) применяется в области неоднородной концентрации. Оно по-прежнему является фундаментальным свойством транспорта, связанным с подвижностью соотношением ( 5 - 4), однако больше не определяет долю тока, переносимую каким-либо ионным компонентом. Тем не менее число переноса сохраняет свое численное значение, например / 0 363 в 0 1 М растворе сульфата меди. Коэффициент D оказывается коэффициентом диффузии сульфата меди, определяющим скорость, с которой сульфат меди диффундировал бы в отсутствие тока. Он имеет промежуточное значение между коэффициентами диффузии ионов меди и сульфата. [26]
Остается обсудить одно важное наблюдение. Единственное доказательство невыполнения уравнения ( 5) получено при давлениях 3 5 и 7 мм рт. ст. для поглощения свыше 65 jis. Выше этой точки поглощение протекает с меньшей скоростью, чем это требуется уравнением. Этот эффект можно объяснить насыщением поверхностных слоев вакансиями. Захват положительных дырок в вакантных центрах должен также усложнять процесс. Вакансии, образуемые во время химического присоединения кислорода, могут быть заполнены при диффузии ионов меди ( 1) с поверхности раздела металл - окисел. При 20 эта диффузия чрезвычайно мала, и, вероятно, химическое присоединение при высоких давлениях газа должно привести к быстрому насыщению поверхностных слоев вакансиями. Однако с повышением температуры точка насыщения смешается в сторону высоких значений q, так как тогда в единицу времени большее число вакансий способно диффундировать с поверхности. Начальная скорость поглощения в этом случае оказывается сравнимой со скоростью, полученной в опытах при высоких давлениях для которых наблюдали невыполнимость уравнения. [27]
Страницы: 1 2