L-изолейцина
Cтраница 1
L-изолейцина из L-треони-на, включающая пять ферментативных реакций. [1]
О том, что такая рацемизация ( или енолизация) не происходит быстро при любых условиях, свидетельствуют наблюдения, показавшие, что L-изомер а-кето-р-метилвалерьяновой кислоты ( соответствующий L-изолейцину и алло - В-изолейцину) более эффективно обеспечивает рост молодых крыс [559] и некоторых бактерий [560], чем оптический антипод этой кетокислоты. Щаве-левоянтарная кислота теоретически может существовать в двух оптически активных формах, но ввиду склонности этой кислоты к енолизации разделение изомеров будет, по-видимому, затруднено. Между тем не исключена возможность, что лишь один из изомеров щавелевоянтарной кислоты метаболически активен. [2]
Как же в клетке регулируется активность ферментов. Мы уже видели, как избыток продукта реакции ( L-изолейцина) подавляет активность фермента, катализирующего первую реакцию в цепи биосинтеза; этого вполне достаточно для полной остановки всего процесса. Такая система регуляции в высшей степени экономична и эффективна, она не требует практически никакой затраты энергии ибо, коль скоро первый фермент уже имеется ( синтезирован), то подавление его действия аминокислотой не требует усилий, оно и вне клетки протекает легко, без подвода энергии. Если провести аналогию с техникой, то ясно, что, например, завод, в котором процессы управления осуществлялись бы при помощи реле, не требующих для своего действия затраты энергии, превосходил бы по эффективности любое из известных промышленных предприятий. Схема регуляции биосинтеза L-изолейцина - это лишь один из примеров подобного рода; аналогичные системы обратной связи направляют в клетке образование и других аминокислот, витаминов и иных важных соединений, в том числе пуриновых и пиримидиновых оснований. [3]
 |
Зависимость между образованием L-глутаминовой кислоты у Corynebacterium glutamicum и содержанием биотина в среде. ( Huang H. Т., Progr. indust. Microbiol., 5, 57. [4] |
Мутанты, нуждающиеся в гомосерине, при подходящих условиях выделяют до 20 г L-лизина на 1 л среды. Другие мутанты С, glutamicum, а также представители семейств Enterobacteriaceae и Pseudomonadaceae служат продуцентами L-гомосерина, L-валина, L-изолейцина, L-триптофана, L-тирозина и других аминокислот. [5]
В основу метода получения В Ь - изолейцина положен ги-дантоиновый синтез по способу Бухерера [1] п Штреккера [2], состоящий в превращении альдегида в циангидрин, дающий при обработке карбонатом аммония замещенный гидантоин. При гидролизе последнего едкими щелочами образуется аминокислота. Этот метод может быть положен в основу промышленного способа получения D. L-изолейцина, так как CHI технологически удобен и дает высокий выход аминокислоты. [6]
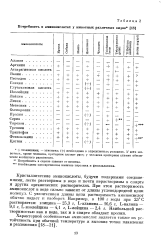 |
Потребность в аминокислотах у животных различных видов. [7] |
Кристаллические аминокислоты, будучи полярными соединениями, легко растворимы в воде и почти нерастворимы в спирте и других органических растворителях. При этом растворимость аминокислот в воде сильно зависит от длины углеводородной цепи молекул. С увеличением длины цепи растворимость аминокислот обычно падает и наоборот. Например, в 100 г воды при 25 С растворяется: глицина - 25 3 г, L-аланина - 16 6 г, L-валина - 9 1 г, L-изолейцина - 4 1 г, L-лейцина - 2 4 г. Наибольшей растворимостью как в воде, так и в спирте обладает пролин. [8]
Страницы: 1