Группа - лантанид
Cтраница 3
Закон Мозли является прежде всего блестящим подтверждением правильности установленных на основании периодической системы порядковых номеров. Далее, на его основе представилась возможность проверить в сомнительных случаях, правильно ли, например, были классифицированы трудноразличимые между собой химические элементы группы лантанидов и имеются ли достаточные основания признавать некоторые из них самостоятельными элементами. [31]
Закон Мозли является прежде всего блестящим подтверждением правильности установленных на основании периодической системы порядковых номеров. Далее, на его основании представилась возмржность проверить в сомнительных случаях, правильно ли, например, были классифицированы трудно различимые между собой химические элементы группы лантанидов и имеются ли достаточные основания признавать некоторые из них самостоятельными элементами. [32]
Закон Мозли является прежде всего блестящим подтверждением правильности установленных на основании периодической системы порядковых номеров. Далее, на его основании представилась возможность проверить в сомнительных случаях, правильно ли, например, были классифицированы трудно различимые между собой химические элементы группы лантанидов и имеются ли достаточные основания признавать некоторые из них самостоятельными элементами. [33]
Важной характеристикой РЗЭ является радиус их ионов: как видно из табл. 29 и рис. 24, величины радиусов сперва увеличиваются - при переходе от скандия к иттрию и лантану, а затем, начиная с церия, постепенно уменьшаются вплоть до лютеция. Это явление, известное под названием лантанидного сжатия и объясняющееся уплотнением не наружных, а глубже лежащих электронных слоев, приводит к тому, что ионы последних элементов группы лантанидов имеют практически такой же радиус, как иттрий. [34]
Слоистое в энергетическом отношении строение атомов, обнаруживающееся в структуре рентгеновских спектров, как уже упоминалось, очень важно для правильного понимания природы главных групп периодической системы. Знакомство с этим строением в той мере, в какой оно отражается в тонкой структуре рентгеновских спектров, обнаруживающей подразделение отдельных электронных оболочек, позволяет понять также и особенности строения побочных подгрупп периодической системы, включая и группы лантанидов и актинидов. [35]
Слоистое в энергетическом отношении строение атомов, обнаруживающееся в структуре рентгеновских спектров, как уже упоминалось, очень важно для правильного понимания природы главных групп периодической системы. Знакомство с этим строением в той мере, в какой оно отражается в тонкой структуре рентгеновских / спектров, обнаруживающей подразделение отдельных электронных оболочек, позволяет понять также и особенности строения побочных подгрупп периодической системы, включая и группы лантанидов и актинидов. [36]
Много опытов было поставлено с целью выяснения вопроса о возможном высшем состоянии окисления кюрия. С точки зрения актинидной теории кюрий занимает положение, совершенно аналогичное положению гадолиния в ряду лантанидов. В группе лантанидов элементы, непосредственно предшествующие гадолинию и следующие за ним, имеют несколько состояний окисления. Гадолиний имеет наполовину заполненную 4 / - оболочку, а конфигурация 4 / 7 необычайно устойчива. Европий, редкоземельный элемент, непосредственно предшествующий гадолинию, приобретает конфигурацию 4 / 7 в состоянии окисления 2; для тербия то же самое осуществляется в состоянии окисления 4 По этой аналогии для кюрия, имеющего конфигурацию 5 / 7, можно ожидать Единственного состояния окисления 3, так же как и у гадоли - ния. В действительности, берклий можно окислить до состояния 4 значительно легче, чем тербий, тогда как америций в двухвалентном состоянии не существует, возможно вследствие большей относительной устойчивости высших состояний окисления актинидов по сравнению с лантанидами. Одной из важнейших проверок правильности теории актинидов является состояние окисления кюрия. [37]
Семейство редких земель, или лантанидов, образует особую группу элементов, химические свойства которых очень сходны. Валентность их обычно равна 3; редко встречающиеся значения 2 и 4 имеют место главным образом для тех ионов, оболочки которых становятся при этом либо пустыми, либо заполненными наполовину, либо полностью заполненными. Существенная особенность группы лантанидов состоит в заполнении 4 / - оболочки; лишь в некоторых исключительных случаях электрон охотнее входит в Sd-оболочку. [38]
Хорошо известно, что у легких элементов ( Z 1, 2, 3, 4) могут заполняться только s - термы. Заполнение р-термов начинается с бора ( Z5), что полностью совпадает с теоретическими данными. Однако в согласии с теорией ее заполнение должно быть отодвинуто и начинается лишь у церия ( Z - 58), образуя группу лантанидов. [39]
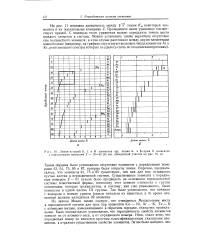 |
Линии а-серий К, L и М элементов ( о. линии а - и р-серии К элементов, с порядковыми номерами Z 19 - 30 ( б ( обведенный участок на 10, а. [40] |
Таким образом было установлено отсутствие элементов с порядковыми номерами 43, 61, 75, 85 и 87, которые были открыты позже. Впрочем, предполагалось, что элементы 43, 75 и 85 существуют, так как для них оставались пустые клетки в периодической системе. Существование элемента с порядковым номером Z 61 нельзя было предвидеть на основании периодической системы классической формы, поскольку этот элемент относится к группе лантанидов, которые трехвалентны, и поэтому, как уже указывалось, были помещены в одной клетке III группы. Так было установлено, что начиная с водорода и кончая ураном ( самым тяжелым из известных в то время элементов) должны находиться 92 элемента. [41]
 |
Припои из сплавов системы Ag-Си - Sb. [42] |
При выборе таких припоев более перспективны в качестве основы пластичные металлы с температурой плавления выше 600 С. Металл - основа таких припоев - согласно анализу существующих диаграмм состояния не должен иметь температуру плавления выше 1100 С. В связи с этим выбор основы для таких прийоев ограничен, это металлы первой группы: серебро, медь, золото с температурами плавления от 960 до 1083 С, а также некоторые металлы группы лантанидов с температурами ликвидуса в интервале 804 - 1070 С. [43]
Оказывается, что теперь 4 / - оболочка несколько более устойчива, чем Sd-оболочка, так что у следующих четырнадцати элементов электроны заполняют 4 / - оболочку, пока она целиком не застроится у атома лютеция. Поскольку у La и у Lu d - оболочка заполнена лишь частично, а все остальные оболочки полностью, оба эти элемента можно было бы отнести к d - rpyn - пе. Однако судя по химическим и физическим свойствам, все 15 элементов от La ( Z57) до Lu ( Z71) ведут себя аналогично; лантан можно считать родоначальником этой группы, которую называют группой лантанидов. Химические свойства этих элементов будут рассмотрены в гл. Следует отметить, что иттрий и скандий по своим свойствам заметно отличаются от обычных переходных элементов й ( - группы. Иттрий в значительной мере, а скандий во многом напоминает лантаниды. Поэтому оба элемента будут рассмотрены также в гл. [44]
Таблица Менделеева исходит из того, что связи и соотношения между элементами чрезвычайно разнообразны и отнюдь не однотипны; поэтому она не заключает каждый элемент в отдельную клетку, что привело бы к признанию равноценности всех мест элементов, а тем самым к признанию однотипности всех отношений между ними. Наоборот, в зависимости от степени химического сходства элементов и близости их атомных чисел ( или атомных весов) менделеевская таблица помещает в одну клетку по одному, по два, по три и даже более элементов. Далее, она учитывает, что внутри больших периодов существует дополнительная, менее резко выраженная периодичность у атомов. Эту добавочную периодичность менделеевская таблица выражает тем, что подразделяет длинный период на два ряда, сдваивая затем эти последние. Наконец, установлено, что группа лантанидов, редкоземельных элементов, также обнаруживает известную периодичность, еще менее резко выраженную Ч В соответствии с этим менделеевская таблица помещает лантаниды в одну клетку и располагает их там согласно их собственной периодичности в два ряда. [45]
Страницы: 1 2 3