Группа - молекула - вода
Cтраница 1
Группы молекул воды в полостях каркасных структур размещаются, как в пузырьках. [1]
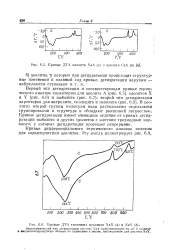 |
Кривые ДТА цеолита NaA ( я н цеолита СаА ( б.| Кривые ДТА типичных цеолитов NaX ( а и NaY ( б. [2] |
В цеолитах второй группы молекулы воды расположены отдельными группировками в структуре и обладают различной летучестью. Кривые дегидратации имеют очевидные отличия от кривых дегидратации шабазита и других цеолитов с жестким трехмерным каркасом, у которых дегидратация протекает непрерывно. [3]
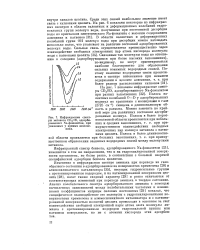
Для того чтобы установить природу различий между группами молекул воды, были исследованы некоторые средние по времени структурные и энергетические свойства. Рассмотрим сначала средние свойства, относящиеся к энергетике связи. Представляют интерес прочность водородных связей между различными молекулами растворителя, полные энергии взаимодействия в присутствии и в отсутствие растворенного вещества и число водородных связей, приходящихся на каждую молекулу. На рис. 2.9 представлены рассчитанные распределения для энергий взаимодействия пар вода - вода. Каждая кривая дает вероятность Р ( к) наблюдения пары молекул с энергией взаимодействия е, если рассматриваются все пары при расстояниях между молекулами до 8 А; кривые нормированы так, что интеграл под каждой равен единице. Три различных распределения соответствуют: 1) парам всех видов в системе; 2) всем парам, которые включают по крайней мере одну молекулу неполярного класса, и 3) всем парам, которые включают по крайней мере одну молекулу полярного класса. Пик при е 0 включает относительно большое число пар, которые разделены довольно значительным расстоянием и которые поэтому имеют очень низкие энергии взаимодействия; число таких пар конечно из-за конечных размеров рассчитываемой ячейки. [4]
Наконец, полоса поглощения 3668 см - была отнесена к колебаниям ОН - групп молекул воды, взаимодействующих с П - электронами ароматического-кольца пиридина. [5]
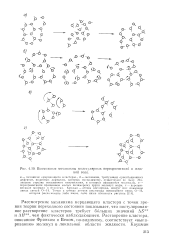 |
Возможные механизмы молекулярных переориентации в жидкой воде. [6] |
Маленькие стрелки показывают направления, в которых вращаются молекулы, в - переориентация вращением малых полимерных групп молекул воды, г - переориентация молекул п пустотах. [7]
Гидролиз солей - взаимодействие солей с водой, приводящее к присоединению протона Н молекулы воды к аниону кислотного остатка и ( или) групп ОН молекулы воды к катиону металла. Гидролизу подвергаются соли, образованные катионами, соответствующими слабым основаниям, и анионами, соответствующими слабым кислотам. [8]
Высказано предположение о том, что адсорбированные молекулы воды могут образовывать водородные связи как с водородом, так и с кислородом поверхностных силанолъных групп [20], При этом полоса поглощения 3450 см-1 приписывается колебаниям групп ОН молекул воды, участвующих в образовании водородной связи через атомы кислорода поверхностных гидроксильных групп, а полоса 3665 см-1 - колебаниям не участвующих в образовании водородной связи групп ОН тех же молекул воды. Таким образом, спектральное проявление адсорбции молекул; воды объясняется только образованием водородных связей с си-ланольными группами поверхности. [9]
Среди этих связей наибольшее значение имеет связь с катионами цеолита. В области валентных и деформационных колебаний групп ОН молекул воды при десорбции можно наблюдать несколько полос, что указывает на различие состояний адсорбированных молекул воды. [11]
Бимолекулярные константы скорости реакций e q примерно на порядок меньше констант скорости реакций ионов На, которые, как показали Эйген и др. [38], зачастую лежат в пределах от 1011 до 1012 см. / сек и для которых предполагается наличие туннельного эффекта в среде с водородными связями. Вместо этого более естественно считать, что электрон связан с группой молекул воды, многие из которых могут двигаться с ним во время его диффузионных перемещений. [12]
Обнаружена нелинейная зависимость между смещением максимума полосы валентных колебаний ОД-трупп в Н - ком-плексах относительно его положения в инертном растворителе и соответствующим сдвигом полосы ОН-группы молекул полутяжелой воды. Найденная зависимость дает экспериментальное доказательство спаривания валентных колебаний ОН и ОД - групп молекулы полутяжелой воды. [13]
Явление гидратации играет большую роль в химии водных растворов. Оно состоит в том, что ион в растворе собирает вокруг себя группу молекул воды, которые довольно плотно к нему прилегают. [14]
В наших опытах при нагревании образцов от - 30 до 100 - J - 150 С при неизменном дублетном расщеплении ширина отдельных компонент уменьшалась примерно в полтора-два раза. Это означает, что при движении вдоль каналов структуры цеолитов 2 - й группы молекулы воды перемещаются параллельно самим себе ( не кувыркаются), в соответствии с наличием предполагаемого электрического поля. [15]
Страницы: 1 2