Группа - реакция
Cтраница 3
Существует группа реакций, в которых гидрид-ион переносится от атома углерода. Связь углерод-водород имеет низкую полярность и мало склонна к разрыву, требуемому для гидридного переноса. Такие реакции обычно протекают через циклические переходные состояния, в которых новые С - Н - связи образуются одновременно с разрывом старых. Гидридпый перенос облегчается за счет высокой плотности заряда па атоме углерода, служащем донором гидрид-иона. Реакция Канниц-царо - катализуемое основаниями диепропорциоштрование альдегидов - является одним из примеров подобных реакций гидридного переноса. [31]
Эта группа реакций лежит в основе большинства способов получения алкенов. [32]
Эта группа реакций лежит в основе наи-юлее широко используемых способов получения алкенов. [33]
Вторая группа реакций кислот связана со специфическими особенностями различных кислот и подразделяется на два типа: реакции, приводящие к образованию нерастворимых солей, и окислительно-восстановительные превращения. [34]
Для групп реакций ( Си; р; 49 Мэв), ( Си; р; 340 Мэв), ( Си; d; ISO Mas) и ( Cu; a; 380 Мэв приведенные в таблице значения параметров Я, Q, К и S дают значения отношений сечений образования ядер-продуктов и сечений образования изотопа Cu6J, выбранного в качестве репера; для группы реакций ( As; d; ISO Мэв) в качестве подобною репера выб; a: i As7, Во всех остальных случаях сечения рассчитываются в миллибариах. [35]
Вторую группу реакций составляют различные методы окисления. Хотя третичные фосфины, особенно с алкильными заместителями, легко окисляются кислородом воздуха, эту реакцию из-за трудности ее контроля редко применяют для получения фосфиноксидов. В качестве окислителей широко используют другие реагенты, в том числе оксиды металлов, азота, а также органические и неорганические пероксиды. [36]
Вторую группу реакций используют для производства оксидов хлора, имеющих практическое применение. Например, широко применяемый в окислительно-отбеливающих процессах диоксид хлора С1С2 получают при восстановлении солей хлорноватой кислоты НСЮ3 диоксидом серы SOa, метанолом СН3ОН, хлоридом водорода и другими восстановителями. [37]
Вторую группу реакций замыкания циклов, которую характеризует внутримолекулярное ацилирование, удобно разделить на две подгруппы: 1) реакции арилкарбоновых кислот и 2) реакции - или т-арилзамещенных алифатических кислот. [38]
В группе реакций ( ч) удобными источниками карбенов и нитронов являются диазо соединения и азиды. При фотолизе тех и других в большинстве случаев образуются синглетные частицы, которые за счет спиновой инверсии при столкновении могут перейти в триплетное состояние. При сенсибилизированном фо-толиве образуются непосредственно частицы в триплетном состоянии. [39]
В группе реакций гидрирования следует различать реакции присоединения водорода к диенам, алкенам, ароматическим углеводородам. Эти реакции, протекая обычно по сходным механизмам, могут значительно различаться между собой по скорости, которая определяется, с одной стороны, строением гидрируемого вещества, а с другой - свойствами катализатора, в первую очередь его химическим составомг. Наиболее общей схемой механизма реакции гидрирования является представление о хемосорбции гидрируемого вещества и водорода на поверхности катализатора и их последующем взаимодействии. [40]
Второй группой реакций, характерных для 4-арнлфуроксанов, является действие восстановителей. Оно может протекать в двух разных направлениях: разрыв фуроксанового кольца до глнокснмиои группировки либо отрыв в нециклического атома кислорода с сохранением фуразанового кольца. [41]
Второй группой реакций окисления является окисление ме-тильных и метиленовых групп. В качестве окислителей при этих реакциях употребляются перекись марганца, перекись свинца и тетраацетат свинца. [42]
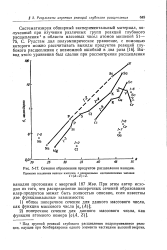 |
Сечения образования продуктов расщепления ванадия. [43] |
Под группой реакций глубокого расщепления подразумеваются реакции, идущие при бомбардировке одного элемента частицами высокой энергии. [44]
Есть еще группа реакций, в которых спирты ведут себя аналогично воде. Это реакции взаимодействия с галогенидами фосфора, которые мы рассмотрим на примере треххлористого фосфора. [45]
Страницы: 1 2 3 4