Группа - периодическая система
Cтраница 3
Металлы групп I-III периодической системы образуют положительные ионы, число элементарных зарядов которых равно номеру группы элемента; таким образом, степень окисления непереходных металлов совпадает с номером их группы. [31]
Часть группы Периодической системы элементов Д. И. Менделеева, содержащая элементы с аналогичной структурой внещних электронных оболочек. [32]
Восьмую группу периодической системы составляют переходные металлы железо, кобальт, никель, рутений, родий, палладий, осмий, иридий и платина, которые расположены в трех триадах. Триады VIII группы образуют элементы наиболее сходные между собой. [33]
Эту группу Периодической системы составляют элементы углерод С, кремний Si, германий Ge, олово Sn и свинец РЬ. По электроотрицательности и химическим свойствам элементы С и Si относятся к неметаллам, элементы Ge, Sn и Pb-к амфотерным элементам, металлические свойства которых возрастают при увеличении порядкового номера и уменьшении степени окисления. [34]
В группу IVa периодической системы входят элементы титан, цирконий, гафний и торий. [35]
VI группе периодической системы, исправил атомные веса иттрия, церия и других редкоземельных элементов. [36]
IV группе периодической системы Менделеева. Однако установление постоянной четырехвалентное углерода во второй половине XIX века было важным событием. В то время, когда уже были известны формулы многих органических веществ, представления о валентности углерода были еще весьма смутны. Валентность часто определяли по числу атомов водорода, способных присоединиться к атому данного элемента. Были известны углеводороды с формулой С2Нг, С2Н4, CjHe, CjHa, и валентность углерода казалась переменной. Полагали, что это находится в соответствии с переменяой валентностью других элементов. [37]
Между группами периодической системы и валентностью существует тесная связь. [38]
В группах периодической системы энергия сродства к электрону и ионизационный потенциал убывают сверху вниз, что приводит к возрастанию восстановительной активности и к уменьшению окислительной в этом направлении. Это позволяет сделать следующий общий вывод: в химическом поведении простых веществ, составленных из атомов элементов, располагающихся в левой нижней половине периодической системы, преобладают восстановительные свойства, в то время как в простых веществах, составленных из атомов элементов правой верхней половины периодической системы, на первый план выдвигаются окислительные свойства. Иными словами, восстановительные свойства преобладают в поведении простых веществ, являющихся металлами, а окислительные свойства преобладают в поведении неметаллов. Разительные примеры в этом отношении - свойства щелочных металлов, с одной стороны, и свойства галогенов, с другой. [39]
В группах периодической системы у р-элементов е увеличением порядкового номера заметно усиливаются восстановительные свойства. [40]
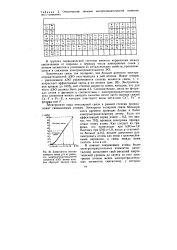 |
Зависимость степени ионности связи q / e от разности электроотрицательноетей элементов АЭО, атомы которых образуют данную связь. [41] |
В группах периодической системы имеется корреляция между увеличением от периода к периоду числа электронных слоев у атомов элементов и усилением их металлических свойств, проявляющихся в снижении электроотрицательности ЭО. [42]
Металлы восьмой группы периодической системы, а также медь и хром поглощают водород, но не образуют с ним химических соединений. [43]
II А группы Периодической системы, взаимодействуя с азотом, образуют нитрид, при гидролизе которого получаются гидроксид металла и аммиак. [44]
Ни одна группа периодической системы элементов не имеет столь близкого отношения к теме этой книги, как главная подгруппа VIII группы - инертные газы. Большинство элементов этой подгруппы помогают сохранять вещества и материалы в чистом виде, участвуют в процессах их получения, обработки, использования. Естественно, что эти стражи-хранители чистоты в противоатмосферной броне сами должны отличаться безукоризненной чистотой. Быстрый рост их производства в последние годы свидетельствует об увеличении выработки чистых веществ. [45]
Страницы: 1 2 3 4